题目内容
15.设nA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 标准状况下,22.4 L CCl4含有4nA个Cl原子 | |
| B. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| C. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| D. | 常温常压下,23 gNO2、N2O4混合气体中含有nA个氧原子 |
分析 A、标况下四氯化碳为液态;
B、求出过氧化钠的物质的量,然后根据1mol过氧化钠和水反应时转移1mol电子来分析;
C、溶液体积不明确;
D、NO2、N2O4的最简式均为NO2;
解答 解:A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和原子个数,故A错误;
B、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠和水反应时转移1mol电子,故0.1mol过氧化钠转移0.1mol电子即0.1nA个,故B错误;
C、溶液体积不明确,故溶液中的钠离子的个数无法计算,故C错误;
D、NO2、N2O4的最简式均为NO2,故23g混合物中含有的NO2的物质的量为n=$\frac{23g}{46g/mol}$=0.5mol,故含1mol氧原子即nA个,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
5.除去下列溶液中的杂质(括号内为杂质)所用的试剂或方法不正确的是( )
| A. | FeCl2溶液【FeCl3】:加足量铁粉 | B. | NaCl溶液【Na2SO4】:用Ba(OH)2溶液 | ||
| C. | Na2CO3固体【NaHCO3】:加热 | D. | 铁粉【铝粉】:用NaOH溶液 |
6.下列有关溶液中粒子浓度的关系式中一定不正确的是( )
| A. | 在常温下,0.10mol•L-1Na2CO3溶液25mL 用0.10mol•L-1盐酸滴定.当滴定到消耗20mlHCl时所得溶液中离子浓度间的关系有:5c(Cl-)=4c(HCO3-)+4c(CO32-)+4c(H2CO3) | |
| B. | 常温下,pH=12的氨水与pH=2的盐酸等体积混合溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| C. | 25℃时,0.1 mol•L-1pH=4.5的NaHSO3溶液中:c(HSO3-)>c(H2SO3)>c(SO32-) | |
| D. | 常温下,等浓度的CH3COONa和CH3COOH混合溶液:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L CCl4中共价键数目为4NA | |
| B. | 22.4 L O2和N2的混合气体中一定含有的原子数为2NA | |
| C. | 常温常压下,6 g NO2和40 g N2O4混合气体中的原子总数为3NA | |
| D. | 25℃时,1mol•L-1醋酸溶液中所含CH3COOH分子总数一定小于NA |
10.归纳与推理是化学学习常用的方法.下列推理正确的是( )
| A. | 因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2 | |
| B. | 因为Mg可以与水反应放出H2,所以Ca也可以与水反应放出H2 | |
| C. | 因为CO2的水溶液可以导电,所以CO2是电解质 | |
| D. | 因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性 |
20.下列有关说法错误的是( )
| A. | 室温下的某 NaF 溶液中,c(H+)=1×10-10 mol?L-1,说明 NaF 使水的电离减弱 | |
| B. | Mg 在空气中燃烧时发出耀眼的白光,一部分化学能转化为光能 | |
| C. | 纯碱溶于热水中去污效果增强,说明纯碱的水解是吸热反应 | |
| D. | 反应 N2(g)+3H2(g)═2NH3(g)(△H<0)达平衡后,降低温度,正、逆反应速率都减小,平衡向正反应方向移动 |
7.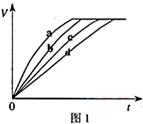 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能
( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能 | 组别 | c(HCl)(mol•L-1) | 温度(℃) | 状态 |
| A | 2.0 | 25 | 块状 |
| B | 2.5 | 30 | 块状 |
| C | 2.5 | 50 | 粉末状 |
| D | 2.5 | 50 | 块状 |
| A. | D-C-A-B | B. | C-D-B-A | C. | A-B-C-D | D. | A-B-D-C |
4.下列各项中表达正确的是( )
| A. | H、D、T表示同一种核素 | B. | 次氯酸电子式 | ||
| C. | F原子结构示意图: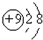 | D. | CH4分子的球棍模型: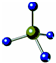 |
