题目内容
在下列化学反应中,既有离子键、极性键断裂,又有离子键、极性键形成的是( )
| A、Na2O+H2O═2NaOH |
| B、SO2+H2O═H2SO3 |
| C、Cl2+H2O═HCl+HClO |
| D、4Li+O2═2Li2O |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,同种非金属所以之间易形成非极性键,不同非金属元素之间易形成极性键,但铵根离子和酸根离子之间存在离子键.
解答:
解:A.该反应中,Na2O中离子键断裂、H2O中极性键断裂、NaOH中离子键和极性键形成,故A正确;
B.该反应中只有极性键的断裂和形成,故B错误;
C.该反应中氯气中非极性断裂、水分子中极性键断裂,HCl、HClO分子中极性键形成,故C错误;
D.该反应中只有金属键、非极性共价键的断裂和离子键的形成,故D错误;
故选A.
B.该反应中只有极性键的断裂和形成,故B错误;
C.该反应中氯气中非极性断裂、水分子中极性键断裂,HCl、HClO分子中极性键形成,故C错误;
D.该反应中只有金属键、非极性共价键的断裂和离子键的形成,故D错误;
故选A.
点评:本题考查了化学键类型的判断,难度不大,注意金属元素和非金属元素之间存在的化学键不一定是离子键,如氯化铝中氯元素和铝元素之间以共价键结合.

练习册系列答案
相关题目
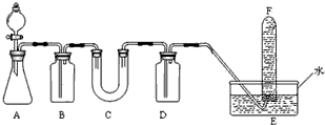
 如图是用实验室制得的乙烯(C2H5OH
如图是用实验室制得的乙烯(C2H5OH | 浓硫酸 |
| 170℃ |
| A、装置①和装置③中都盛有水,其作用相同 |
| B、装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同 |
| C、产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出 |
| D、制备乙烯和生成1,2-二溴乙烷的反应类型分别是消去反应和加成反应 |

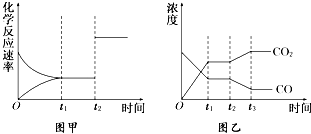 已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;
已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;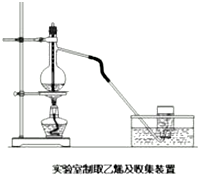 实验室常用下面装置制备乙稀,请回答下列问题:
实验室常用下面装置制备乙稀,请回答下列问题:
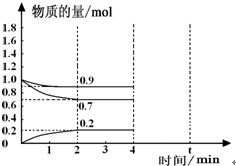 工业上合成合成氨的热化学方程式如下:
工业上合成合成氨的热化学方程式如下: