题目内容
 已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;
已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2,
在温度973K和1173K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
(3)要使反应③在一定条件下建立的平衡向正反应方向移动同时υ正增大可采取的措施有
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂 E.设法减小平衡体系中的CO的浓度
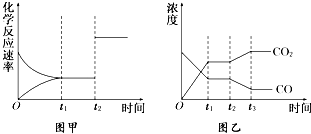
(4)如图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是
②图乙中t2时刻发生改变的条件是
(5)在830℃温度下,反应③的K值为1,在2L的密闭容器中,加入1mol CO2和3mol H2充分反应达平衡时,CO平衡浓度为
考点:化学平衡的计算,化学平衡的影响因素,化学反应速率与化学平衡图象的综合应用
专题:化学平衡专题
分析:(1)反应①中,升高温度,化学平衡常数增大,说明平衡向正反应方向移动,升高温度平衡向吸热反应方向移动;
(2)将方程式①-②得反应③:CO2(g)+H2(g)?CO(g)+H2O(g),K3=
=
.
=
;
升高温度根据平衡常数变化确定反应热;
(3)该反应是反应前后气体体积不变的吸热反应,平衡向正反应方向移动同时υ正增大,可以采用升高温度的方法;
(4)①图甲中t2时刻,正逆反应速率同等程度的增大,平衡不移动,可以采用使用催化剂、增大压强的方法;
②图乙中t2时刻,二氧化碳浓度增大、CO浓度减小,平衡向逆反应方向移动;
(5)在830℃温度下,反应③的K值为1,开始时c(CO2)=
=0.5mol/L、c(H2)=
=1.5mol/L,
设平衡时参加反应的氢气浓度为xmol/L,
CO2(g)+H2(g)?CO(g)+H2O(g)
开始0.5mol/L 1.5mol/L 0 0
反应xmol/L xmol/L xmol/L xmol/L
平衡(0.5-x)mol/L(1.5-x)mol/L xmol/L xmol/L
化学平衡常数K=
=1,x=0.375,
据此计算平衡时CO浓度、氢气的转化率;
温度不变,化学平衡常数不变,据此进行计算.
(2)将方程式①-②得反应③:CO2(g)+H2(g)?CO(g)+H2O(g),K3=
| c(CO).c(H2O) |
| c(CO2).c(H2) |
| c(CO) |
| c(CO2) |
| 1 | ||
|
| K1 |
| K2 |
升高温度根据平衡常数变化确定反应热;
(3)该反应是反应前后气体体积不变的吸热反应,平衡向正反应方向移动同时υ正增大,可以采用升高温度的方法;
(4)①图甲中t2时刻,正逆反应速率同等程度的增大,平衡不移动,可以采用使用催化剂、增大压强的方法;
②图乙中t2时刻,二氧化碳浓度增大、CO浓度减小,平衡向逆反应方向移动;
(5)在830℃温度下,反应③的K值为1,开始时c(CO2)=
| 1mol |
| 2L |
| 3mol |
| 2L |
设平衡时参加反应的氢气浓度为xmol/L,
CO2(g)+H2(g)?CO(g)+H2O(g)
开始0.5mol/L 1.5mol/L 0 0
反应xmol/L xmol/L xmol/L xmol/L
平衡(0.5-x)mol/L(1.5-x)mol/L xmol/L xmol/L
化学平衡常数K=
| x.x |
| (0.5-x).(1.5-x) |
据此计算平衡时CO浓度、氢气的转化率;
温度不变,化学平衡常数不变,据此进行计算.
解答:
解:(1)反应①中,升高温度,化学平衡常数增大,说明平衡向正反应方向移动,升高温度平衡向吸热反应方向移动,所以正反应是吸热反应,故答案为:吸热;
(2)将方程式①-②得反应③:CO2(g)+H2(g)?CO(g)+H2O(g),K3=
=
.
=
,升高温度,K1增大、K2减小,则K3增大,则该反应是吸热反应,故答案为:
;K3=
;吸热;
(3)该反应是反应前后气体体积不变的吸热反应,平衡向正反应方向移动同时υ正增大,可以采用升高温度的方法,故选C;
(4)①该反应是反应前后气体体积不变的吸热反应,图甲中t2时刻,正逆反应速率同等程度的增大,平衡不移动,可以采用使用催化剂、增大压强的方法,
故答案为:增大压强或使用催化剂;
②该反应是反应前后气体体积不变的吸热反应,图乙中t2时刻,二氧化碳浓度增大、CO浓度减小,平衡向逆反应方向移动,可以采用降低温度、分离出氢气的方法,
故答案为:降低温度或从体系中分离出H2;
(5)在830℃温度下,反应③的K值为1,开始时c(CO2)=
=0.5mol/L、c(H2)=
=1.5mol/L,
设平衡时参加反应的氢气浓度为xmol/L,
CO2(g)+H2(g)?CO(g)+H2O(g)
开始 0.5mol/L 1.5mol/L 0 0
反应 xmol/L xmol/L xmol/L xmol/L
平衡(0.5-x)mol/L(1.5-x)mol/L xmol/L xmol/L
化学平衡常数K=
=1,x=0.375,
则平衡时CO浓度=(0.5-0.375)mol/L=0.125mol/L,氢气的转化率=
×100%=25%;
温度不变,化学平衡常数不变,
设平衡时参加反应的CO浓度为ymol/L,开始时c(CO2)=
=1mol/L、c(H2)=
=3mol/L,
CO2(g)+H2(g)?CO(g)+H2O(g)
开始1mol/L 3mol/L 0 0
反应ymol/L ymol/L ymol/L ymol/L
平衡(1-y)mol/L(3-y)mol/L ymol/L ymol/L
化学平衡常数K=
=1,y=0.75,
平衡时c(CO)=0.75mol/L,
二氧化碳体积分数等其物质的量分数=
×100%=6.25%,
故答案为:0.375;25%; 0.75;6.25%.
(2)将方程式①-②得反应③:CO2(g)+H2(g)?CO(g)+H2O(g),K3=
| c(CO).c(H2O) |
| c(CO2).c(H2) |
| c(CO) |
| c(CO2) |
| 1 | ||
|
| K1 |
| K2 |
| c(CO).c(H2O) |
| c(CO2).c(H2) |
| K1 |
| K2 |
(3)该反应是反应前后气体体积不变的吸热反应,平衡向正反应方向移动同时υ正增大,可以采用升高温度的方法,故选C;
(4)①该反应是反应前后气体体积不变的吸热反应,图甲中t2时刻,正逆反应速率同等程度的增大,平衡不移动,可以采用使用催化剂、增大压强的方法,
故答案为:增大压强或使用催化剂;
②该反应是反应前后气体体积不变的吸热反应,图乙中t2时刻,二氧化碳浓度增大、CO浓度减小,平衡向逆反应方向移动,可以采用降低温度、分离出氢气的方法,
故答案为:降低温度或从体系中分离出H2;
(5)在830℃温度下,反应③的K值为1,开始时c(CO2)=
| 1mol |
| 2L |
| 3mol |
| 2L |
设平衡时参加反应的氢气浓度为xmol/L,
CO2(g)+H2(g)?CO(g)+H2O(g)
开始 0.5mol/L 1.5mol/L 0 0
反应 xmol/L xmol/L xmol/L xmol/L
平衡(0.5-x)mol/L(1.5-x)mol/L xmol/L xmol/L
化学平衡常数K=
| x.x |
| (0.5-x).(1.5-x) |
则平衡时CO浓度=(0.5-0.375)mol/L=0.125mol/L,氢气的转化率=
| 0.375mol/L |
| 1.5mol/L |
温度不变,化学平衡常数不变,
设平衡时参加反应的CO浓度为ymol/L,开始时c(CO2)=
| 2mol |
| 2L |
| 6mol |
| 2L |
CO2(g)+H2(g)?CO(g)+H2O(g)
开始1mol/L 3mol/L 0 0
反应ymol/L ymol/L ymol/L ymol/L
平衡(1-y)mol/L(3-y)mol/L ymol/L ymol/L
化学平衡常数K=
| y.y |
| (1-y).(3-y) |
平衡时c(CO)=0.75mol/L,
二氧化碳体积分数等其物质的量分数=
| 1-0.75 |
| 1+3 |
故答案为:0.375;25%; 0.75;6.25%.
点评:本题考查化学平衡的计算、反应热的计算、平衡移动方向的判断等知识点,侧重考查学生分析能力、计算能力,知道外界条件对化学平衡移动的影响,知道化学平衡常数只与温度有关,题目难度中等.

练习册系列答案
相关题目
25℃某气态烃与氧气混合充入密闭容器中,点火爆炸后又恢复到25℃,此时容器内压强为开始时的一半,再经氢氧化钠溶液处理,容器内几乎为真空,该烃的分子式为( )
| A、C2H4 |
| B、C3H6 |
| C、C2H6 |
| D、C5H12 |
在强酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
| A、Ca2+、Na+、NO3-、CO32- |
| B、Mg2+、Cl-、NH4+、SO42- |
| C、K+、Cl-、HCO3-、NO3- |
| D、Ca2+、Na+、Fe3+、NO3- |
在下列化学反应中,既有离子键、极性键断裂,又有离子键、极性键形成的是( )
| A、Na2O+H2O═2NaOH |
| B、SO2+H2O═H2SO3 |
| C、Cl2+H2O═HCl+HClO |
| D、4Li+O2═2Li2O |
下列关于药物的使用,说法正确的是( )
| A、“是药三分毒”,必须按医嘱或药物说明书使用药物,防范不良反应 |
| B、使用青霉素时,直接静脉注射,可以不用进行皮肤敏感试验 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、对于标记“OTC”的药物,必须持有医生的处方才能购买 |