题目内容
 工业上合成合成氨的热化学方程式如下:
工业上合成合成氨的热化学方程式如下:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
(1)请在答卷上画出以上反应过程中体系的能量变化图(进行必要的标注).
(2)工业上采取以下措施能用勒夏特列原理解释的是
A.加入催化剂
B.增大反应容器的压强(50MPa)
C.升高反应的温度(500℃)
D.设法分离产生的氨气
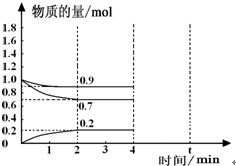
(3)一定温度下,在密闭容器中进行以上反应.容器中0-4minN2、H2和NH3三种气体的物质的量随时间的变化曲线如图所示.
①若容器为体积为2L的恒容容器,则反应开始2分钟 NH3的平均反应速率为
②若容器为体积可变的恒压容器,在4min时往容器中再加入N2和H2各1mol,平衡向
考点:化学平衡的计算,化学平衡移动原理
专题:
分析:(1)根据合成氨的热化学方程式知,合成氨的反应为放热反应,氮气和氢气的总能量高于氨气的总能量;
(2)有化学平衡移动的可以用勒夏特列原理解释,
A、加入催化剂平衡不移动,不能用勒夏特列原理解释;
B、合成氨的反应正向为气体体积减小的反应,增大反应容器的压强(50MPa),平衡正向移动;
C、合成氨的反应为放热反应,升高反应的温度(5000C) 平衡逆向移动,反应物的转化率减小,不能用勒夏特列原理解释;
D、设法分离产生的氨气平衡正向移动,能用勒夏特列原理解释;
(3)①根据公式v=△n/V△t计算;
②若容器为体积可变的恒压容器,在4min时往容器中再加入N2和H2各1mol,反应物的浓度增大,生成物的浓度减小,平衡向右移动,温度未发生变化,平衡常数不变;根据等效平衡知识,反应一段时间后,在t min时再次达到平衡时H2的物质的量为原平衡的2倍.
(2)有化学平衡移动的可以用勒夏特列原理解释,
A、加入催化剂平衡不移动,不能用勒夏特列原理解释;
B、合成氨的反应正向为气体体积减小的反应,增大反应容器的压强(50MPa),平衡正向移动;
C、合成氨的反应为放热反应,升高反应的温度(5000C) 平衡逆向移动,反应物的转化率减小,不能用勒夏特列原理解释;
D、设法分离产生的氨气平衡正向移动,能用勒夏特列原理解释;
(3)①根据公式v=△n/V△t计算;
②若容器为体积可变的恒压容器,在4min时往容器中再加入N2和H2各1mol,反应物的浓度增大,生成物的浓度减小,平衡向右移动,温度未发生变化,平衡常数不变;根据等效平衡知识,反应一段时间后,在t min时再次达到平衡时H2的物质的量为原平衡的2倍.
解答:
解:(1)根据合成氨的热化学方程式知,合成氨的反应为放热反应,氮气和氢气的总能量高于氨气的总能量,故反应过程中体系的能量变化图为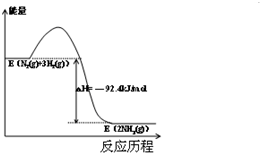 ,故答案为:
,故答案为: ;
;
(2)A、加入催化剂平衡不移动,不能用勒夏特列原理解释,故A错误;
B、合成氨的反应正向为气体体积减小的反应,增大反应容器的压强(50MPa),平衡正向移动,能用勒夏特列原理解释,故B正确;
C、合成氨的反应为放热反应,升高反应的温度(5000C) 平衡逆向移动,反应物的转化率减小,不能用勒夏特列原理解释,故C错误;
D、设法分离产生的氨气平衡正向移动,能用勒夏特列原理解释,故D正确;
故答案为:BD;
(3)①根据公式v=△n/V△t计算;根据图象可知,反应开始2分钟 NH3的物质的量变化为0.2mol,容器的体积为2L,则反应速率v=
=
=0.05mol/(L?min);
故答案为:0.05mol/(L?min);
②若容器为体积可变的恒压容器,在4min时往容器中再加入N2和H2各1mol,反应物的浓度增大,生成物的浓度减小,平衡向右移动,温度未发生变化,平衡常数不变;根据等效平衡知识,反应一段时间后,在t min时再次达到平衡时H2的物质的量为原平衡的2倍.H2在4min-t min时间内物质的量的变化曲线为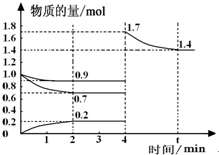 ,故答案为:向右;不变;
,故答案为:向右;不变; .
.
 ,故答案为:
,故答案为: ;
;(2)A、加入催化剂平衡不移动,不能用勒夏特列原理解释,故A错误;
B、合成氨的反应正向为气体体积减小的反应,增大反应容器的压强(50MPa),平衡正向移动,能用勒夏特列原理解释,故B正确;
C、合成氨的反应为放热反应,升高反应的温度(5000C) 平衡逆向移动,反应物的转化率减小,不能用勒夏特列原理解释,故C错误;
D、设法分离产生的氨气平衡正向移动,能用勒夏特列原理解释,故D正确;
故答案为:BD;
(3)①根据公式v=△n/V△t计算;根据图象可知,反应开始2分钟 NH3的物质的量变化为0.2mol,容器的体积为2L,则反应速率v=
| △c |
| △t |
| ||
| 2min |
故答案为:0.05mol/(L?min);
②若容器为体积可变的恒压容器,在4min时往容器中再加入N2和H2各1mol,反应物的浓度增大,生成物的浓度减小,平衡向右移动,温度未发生变化,平衡常数不变;根据等效平衡知识,反应一段时间后,在t min时再次达到平衡时H2的物质的量为原平衡的2倍.H2在4min-t min时间内物质的量的变化曲线为
 ,故答案为:向右;不变;
,故答案为:向右;不变; .
.
点评:本题考查化学反应与能量变化、化学反应速率和化学平衡的计算及图象,旨在考查学生对基础知识的理解掌握,难度中等.

练习册系列答案
相关题目
在下列化学反应中,既有离子键、极性键断裂,又有离子键、极性键形成的是( )
| A、Na2O+H2O═2NaOH |
| B、SO2+H2O═H2SO3 |
| C、Cl2+H2O═HCl+HClO |
| D、4Li+O2═2Li2O |
在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的
,当达到新平衡时,C的浓度为原来的1.9倍.下列说法中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、平衡向逆反应方向移动 |
| C、A的转化率增大 |
| D、C的体积分数增加 |
下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.
相同条件下,有关上述溶液的比较中,正确的是( )
相同条件下,有关上述溶液的比较中,正确的是( )
| A、由水电离的c(H+):①=②>③=④ |
| B、将①、③两种溶液等体积混合后,pH可能不等于7 |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D、向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>② |
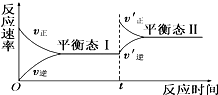 如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )
如图是恒温下化学反应“A(g)+B(g)?C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )| A、平衡态Ⅰ与平衡态Ⅱ的正反应速率相等 |
| B、平衡移动的原因可能是增大了反应物浓度 |
| C、平衡移动的原因可能是增大了压强 |
| D、平衡状态Ⅰ和平衡状态Ⅱ的平衡常数的大小关系为K1<K2 |
下列有关离子的检验方法,正确的是( )
| A、向某溶液加入硫酸酸化的氯化钡溶液,以检验SO42-的存在 |
| B、向某溶液中滴加浓氨水,以检验Al3+的存在 |
| C、用铂丝蘸取某溶液在火焰上灼烧,直接观察火焰颜色,以检验K+的存在 |
| D、向某溶液中加入稀硝酸酸化的硝酸银溶液,以检验Cl-的存在 |
下列能用勒沙特列原理解释的是( )
| A、Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| B、棕红色Br2蒸气加压后颜色变深 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混和气加压后颜色变深 |