题目内容
13.密闭容器中有反应:Mg+2HCl=MgCl2+H2↑ 2s后HCl的浓度由2mol/L减小到1mol/L,求该反应的速率( )| A. | 1mol/(L•s) | B. | 0.5mol/(L•s) | C. | 1.5 mol/(L•s) | D. | 无法计算 |
分析 反应速率表示单位时间内浓度的变化量,即反应速率v=$\frac{△C}{△t}$,据此计算.
解答 解:2s后HCl的浓度由2mol/L减小到1mol/L,则2s后内HCl的化学反应速率=$\frac{2mol/L-1mol/L}{2s}$=0.5mol/(L•s);
故答案为:0.5mol/(L•s).
点评 本题考查反应速率的计算,根据反应速率公式进行计算,注意纯液体、固体浓度一般认为是常数,其浓度在反应中不变.

练习册系列答案
相关题目
3.下列各类有机物:①饱和一元醇 ②饱和一元醛 ③饱和一元羧酸 ④饱和一元醇与饱和一元酸生成的酯 ⑤乙炔的同系物 ⑥苯的同系物 ⑦烯烃的同系物,完全燃烧时产生的水和二氧化碳的物质的量之比恒定的是( )
| A. | ①③⑤⑦ | B. | ①④⑥ | C. | ②③④⑦ | D. | ②③④⑤⑥ |
5.使1mol某烷烃完全燃烧需要消耗氧气5mol,该烷烃的化学式是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
3.25℃把 0.02mol/LCH3COOH溶液和0.01mol/LKOH溶液以等体积混和,则混合液中微粒浓度关系正确的为:(已知?25℃:CH3COOH电离常数是1.76×10-5,CH3COO-水解常数是5.78×10-10;?体积变化忽略不计;)( )
| A. | c (K+)>c (CH3COO-)>c(H+)>c (OH-) | B. | c(K+)=c (CH3COO-)>c (OH-)=c (H+) | ||
| C. | c(K+)+c (H+)═c(CH3COOH)+c (OH-) | D. | c (CH3COOH)+c (CH3COO-)=0.01mol/L |

 .
. .
. .
. ,形成过程
,形成过程 ;
;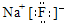 ,形成过程
,形成过程 ;
; ,形成过程
,形成过程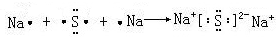 ;
; ;
; ,形成过程
,形成过程 .
.