题目内容
18.写出下列物质的电子式,并用电子式来表示下列物质的形成过程.(1)H2O:电子式
 ,形成过程
,形成过程 ;
;(2)NaF:电子式
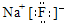 ,形成过程
,形成过程 ;
;(3)Na2S:电子式
 ,形成过程
,形成过程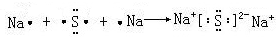 ;
;(4)H2:电子式H:H,形成过程
 ;
;(5)HCl:电子式
 ,形成过程
,形成过程 .
.
分析 首先判断化合物是离子化合物还是共价化合物;
若是离子化合物,其电子式 由阴、阳离子的电子式组合而成,相同的离子不能合并;
若是共价化合物,其电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况.
用电子式表示离子化合物的形成过程,左边写成键原子的电子式,相同的原子可以合并,右边写离子化合物的电子式,相同的离子不能合并,中间用箭号连接,左边用弯箭头表示电子的得失.
解答 解:(1)H2O是共价化合物,氧原子分别与两个氢原子通过一对共用电子对结合,电子式为 ;
;
H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ,
,
故答案为: ;
; ;
;
(2)氟化钠是离子化合物,由氟离子与钠离子构成,电子式: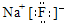 ;
;
NaF为离子化合物,用电子式表示形成过程为 ;
;
故答案为: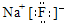 ;
; ;
;
(3)Na2S为离子化合物,由硫离子与钠离子构成,电子式为: ;
;
Na2S为离子化合物,用电子式表示形成过程为: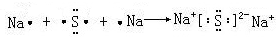 ;
;
故答案为: ;
;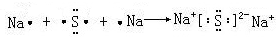 ;
;
(4)H2中H原子间以共价键,即共用电子对结合,电子式为:H:H;
H2中H原子间以共价键,用电子式表示形成过程为: ;
;
故答案为:H:H; ;
;
(5)HCl属于共价化合物,原子间以共用电子对成键,电子式为 ,
,
HCl为共价化合物,用电子式表示形成过程: ;
;
故答案为: ;
; .
.
点评 本题考查了用电子式的书写以及用电子式表示单质、化合物形成过程,题目难度中等,要求学生熟练掌握电子式的概念及表示方法,注意离子化合物、共价化合物电子式的写法.

练习册系列答案
相关题目
8.既属于有机物,又属于酸的是( )
| A. | H2SO4 | B. | CH2=CH2 | C. | CH3COOH | D. | CH3CH2OH |
13.密闭容器中有反应:Mg+2HCl=MgCl2+H2↑ 2s后HCl的浓度由2mol/L减小到1mol/L,求该反应的速率( )
| A. | 1mol/(L•s) | B. | 0.5mol/(L•s) | C. | 1.5 mol/(L•s) | D. | 无法计算 |
3.常温下将0.1mol的Cl2通入0.5L的水中(不计溶液体积变化),制得氯水,关于这份氯水下列说法正确的是( )
| A. | 若不考虑HClO和H20的电离,该溶液中H+的浓度为0.1mol/L | |
| B. | 若在该溶液中加入足量Na0H,则可得到0.1mol的NaClO | |
| C. | 若将此溶液在强光下光照,产生气泡,则气泡主要成分是O2 | |
| D. | 此溶液久置后,由于HClO的大量分解,会导致其pH值升高 |
10.用惰性电极电解下列溶液时在阴阳两极收集到的气体体积比为2:1的是( )
| A. | H2SO4 | B. | HCl | C. | AgNO3 | D. | NaOH |
8.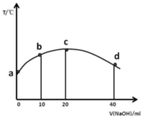 若往20ml 0.01mol/LCH3COOH溶液中逐滴加入一定浓度的烧碱溶液,测的溶液的温度变化如图所示,下列有关说法正确的是( )
若往20ml 0.01mol/LCH3COOH溶液中逐滴加入一定浓度的烧碱溶液,测的溶液的温度变化如图所示,下列有关说法正确的是( )
 若往20ml 0.01mol/LCH3COOH溶液中逐滴加入一定浓度的烧碱溶液,测的溶液的温度变化如图所示,下列有关说法正确的是( )
若往20ml 0.01mol/LCH3COOH溶液中逐滴加入一定浓度的烧碱溶液,测的溶液的温度变化如图所示,下列有关说法正确的是( )| A. | c点时,醋酸的电离程度和电离常数都最大,溶液呈中性 | |
| B. | 若b点混合溶液显酸性,则2c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 混合溶液中水的电离程度:b>c>d | |
| D. | 由图可知,该反应的中和热先增大后减小 |
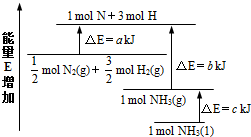 氨气是氮循环中的重要物质,在人类的生产生活中有着广泛的应用.
氨气是氮循环中的重要物质,在人类的生产生活中有着广泛的应用.