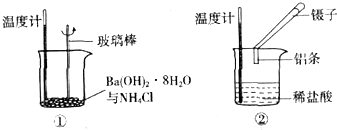
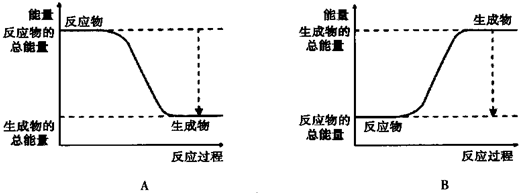
题目内容
13.在一定温度下,在一个容积不变的有催化剂的容器中,通入2molN2和8molH2.已知:N2 (g)+3H2(g)?2NH3(s)△H=-92.2kJ/mol,达到平衡时容器内气体压强为起始时的80%.(1)达到平衡时,N2的转化率为50%.
(2)达到平衡时,容器内NH3的体积分数为25%.
(3)达到平衡时,放出的热量等于(填“大于”、“小于”或“等于”)92.2kJ.
分析 在一定温度下,在一个容积不变的有催化剂的容器中,通入2moL N2和8moL H2,设转化氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):2 8 0
转化量(mol):x 3x 2x
平衡量(mol):2-x 8-3x 2x
达到平衡时容器内气体压强为起始时的80%,则10-2x=10×80%,解得x=1,据此进行计算.
解答 在一定温度下,在一个容积不变的有催化剂的容器中,通入2moL N2和8moL H2,设转化氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):2 8 0
转化量(mol):x 3x 2x
平衡量(mol):2-x 8-3x 2x
达到平衡时容器内气体压强为起始时的80%,则:2+8-2x=(2+8)×80%,解得:x=1,
(1)达到平衡时,N2的转化率为:$\frac{1mol}{2mol}$×100%=50%,
故答案为:50%;
(2)达到平衡时,容器内NH3的体积分数为:$\frac{2mol}{8mol}$×100%=25%,
故答案为:25%;
(3)参加反应的n(N2)=1mol,所以放出的热量为:1mol×92.2kJ•mol-1=92.2kJ,
故答案为:等于.
点评 本题考查化学平衡计算素,题目难度中等,明确压强与气体物质的量的关系为解答关键,注意三段式解题法在化学平衡计算中应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
1.下列分子或离子之间互为等电子体的是( )
| A. | CS2和NO2 | B. | N2和CO | C. | CO2和SO2 | D. | NH3和NH4+ |
18.下列液体混合物中可以用分液漏斗进行分离,且操作时水从分液漏斗的下口流出来的一组是( )
| A. | 苯和水 | B. | 酒精和水 | C. | 溴苯和水 | D. | 硝基苯和水 |
2.碳单质有多种同素异形体,下列有关叙述错误的是( )
| A. | 金刚石硬度很高,用于制作精美首饰 | |
| B. | C60分子可镶入金属钾,用做高温超导体 | |
| C. | 石墨熔沸点高,用做飞船表面隔热材料 | |
| D. | 碳纳米管导电性好,用于制作大规模集成电路 |
3.向氯化铁溶液中加入ag铜粉,完全溶解后再加入b g铁粉,充分反应后过滤得到滤液和固体c g.下列说法正确的是( )
| A. | 若a>c,则滤液中可能含三种金属离子,且b可能小于c | |
| B. | 若a>c,则c g固体中只含一种金属,且b可能大于c | |
| C. | 若a<c,则c g固体含两种金属,且b可能与c相等 | |
| D. | 若a=c,则滤液中可能含两种金属离子,且b可能小于c |
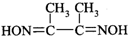 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.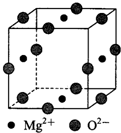
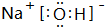 ,CB2的电子式为
,CB2的电子式为 .
.