题目内容
下列有关化学用语使用正确的是( )
A、质量数为35的氯原子:
| ||
B、BaSO4的电离方程式:BaSO4=Ba2++S
| ||
| C、乙烯的结构简式:C2H4 | ||
D、氯原子结构示意图: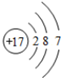 |
考点:核素,原子结构示意图,结构简式,电离方程式的书写
专题:化学用语专题
分析:A.质量数为35的氯原子为:1735Cl;
B.硫酸钡是强电解质,溶于水的部分完全电离;
C.乙烯含有碳碳双键;
D.氯原子质子数为17,核外电子数为17.
B.硫酸钡是强电解质,溶于水的部分完全电离;
C.乙烯含有碳碳双键;
D.氯原子质子数为17,核外电子数为17.
解答:
解:A.质量数为35的氯原子:1735Cl,故A错误;
B.硫酸钡是强电解质,溶于水的部分完全电离,电离方程式为BaSO4═Ba2++SO42-,故B正确;
C.乙烯含有碳碳双键,结构简式为:CH2=CH2,故C错误;
D.氯原子质子数为17,核外电子数为17,故结构示意图为: ,故D正确;
,故D正确;
故选BD.
B.硫酸钡是强电解质,溶于水的部分完全电离,电离方程式为BaSO4═Ba2++SO42-,故B正确;
C.乙烯含有碳碳双键,结构简式为:CH2=CH2,故C错误;
D.氯原子质子数为17,核外电子数为17,故结构示意图为:
 ,故D正确;
,故D正确;故选BD.
点评:本题考查原子符号、电离方程式、结构简式、原子结构示意图等化学用语的使用,难度不大.要注意基础知识的积累.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目
已知在相同状况下,同一化学键断裂需要吸收的能量等于形成该化学键放出的能量.下列说法错误的是( )
| A、电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应 |
| B、H2(g)+F2(g)=2HF(g)△H=-270 kJ/mol,1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
| C、相同状况下,反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应 |
| D、破坏1 mol氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol氯气中的化学键消耗的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ,则Q1+Q2<2Q3 |
下列事实中,能证明硫酸是强电解质的是( )
| A、用连有小灯泡的电路测硫酸溶液的导电性,灯泡较亮 |
| B、能跟锌反应产生氢气 |
| C、1mol/L硫酸溶液中H+浓度为2mol/L |
| D、能与碳酸钠反应放出二氧化碳气体 |
从海水中提取镁的主要步骤
①把贝壳烧成生石灰;
②在海水中加入生石灰,过滤,洗涤沉淀物;
③将沉淀物与盐酸反应,结晶,过滤;
④在氯化氢热气流中加热晶体
⑤电解上述所得盐(熔融条件下)
下列说法不正确的是( )
①把贝壳烧成生石灰;
②在海水中加入生石灰,过滤,洗涤沉淀物;
③将沉淀物与盐酸反应,结晶,过滤;
④在氯化氢热气流中加热晶体
⑤电解上述所得盐(熔融条件下)
下列说法不正确的是( )
| A、上述变化包括分解反应,化合反应,复分解反应类型 |
| B、贝壳烧成生石灰属于吸热反应 |
| C、在氯化氢热气流中干燥晶体的目的是为了抑制阳离子的水解 |
| D、步骤⑤也可以采用电解该盐水溶液的方法 |
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )| A、在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX | ||
| B、根据滴定曲线,可得Ka(HY)≈10-5 | ||
| C、将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) | ||
D、HY与HZ混合,达到平衡时:c(H+)=
|
下列各组物质中最简式相同,但既不是同系物又不是同分异构体的是( )
| A、丙烯和环丙烷 |
| B、甲醛和乙酸 |
| C、乙酸和甲酸甲酯 |
| D、乙醛和乙酸乙酯 |