题目内容
主族元素R的最高价氧化物R2O 4.7g溶于95.3g水中,所得溶液的质量分数为5.6%,R原子核中含有20个中子;主族元素Q,其单质能与水剧烈反应放出O2,并能跟R形成典型的离子化合物RQ.试通过计算求:
(1)写出R和Q在元素周期表中的位置;
(2)将4.7g R2O溶于多少克水中,使每50个水分子溶有1个R+(写出计算过程).
(1)写出R和Q在元素周期表中的位置;
(2)将4.7g R2O溶于多少克水中,使每50个水分子溶有1个R+(写出计算过程).
考点:化学方程式的有关计算,原子结构与元素的性质
专题:计算题,原子组成与结构专题
分析:(1)主族元素Q,其单质能与水剧烈反应放出O2,则Q为F元素,且能跟R形成典型的离子化合物RQ,则R处于ⅠA族,主族元素R的最高价氧化物R2O 4.7g溶于95.3g水中,得到ROH溶液,所得溶液的质量分数为5.6%,则ROH的质量=(4.7g+95.3g)×5.6%=5.6g,令R的相对原子质量为a,则根据R原子守恒:2×
=
,解得a=39,R原子核中含有20个中子,则其质子数为39-20=19,故R为K元素;
(2)根据n=
计算4.7g R2O的物质的量,根据方程式计算参加反应水的物质的量,根据溶液中水分子与R+离子数量关系计算溶液中水的物质的量,两部分相加可得需要水的物质的量,再根据m=nM计算.
| 4.7 |
| 2a+16 |
| 5.6 |
| a+17 |
(2)根据n=
| m |
| M |
解答:
解:(1)主族元素Q,其单质能与水剧烈反应放出O2,则Q为F元素,处于第二周期ⅦA族;
Q能跟R形成典型的离子化合物RQ,则R处于ⅠA族,主族元素R的最高价氧化物R2O 4.7g溶于95.3g水中,得到ROH溶液,所得溶液的质量分数为5.6%,则ROH的质量=(4.7g+95.3g)×5.6%=5.6g,令R的相对原子质量为a,则根据R原子守恒:2×
=
,解得a=39,R原子核中含有20个中子,则其质子数为39-20=19,故R为K元素,处于第四周期ⅠA族,
答:R为K元素,处于第四周期ⅠA族,Q为F元素,处于第二周期ⅦA族.
(2)4.7g K2O的物质的量=
=0.05mol,由K2O+H2O=2KOH可知,0.05molK2O消耗0.05mol水,生成KOH为0.05mol×2=0.1mol,溶液中每50个水分子溶有1个R+离子,则溶液中水的物质的量=0.1mol×50=5mol,故需要水的物质的量=5mol+0.05mol=5.05mol,则需要水的质量=5.05mol×18g/mol=90.9g,
答:需要水的质量为90.9g.
Q能跟R形成典型的离子化合物RQ,则R处于ⅠA族,主族元素R的最高价氧化物R2O 4.7g溶于95.3g水中,得到ROH溶液,所得溶液的质量分数为5.6%,则ROH的质量=(4.7g+95.3g)×5.6%=5.6g,令R的相对原子质量为a,则根据R原子守恒:2×
| 4.7 |
| 2a+16 |
| 5.6 |
| a+17 |
答:R为K元素,处于第四周期ⅠA族,Q为F元素,处于第二周期ⅦA族.
(2)4.7g K2O的物质的量=
| 4.7g |
| 94g/mol |
答:需要水的质量为90.9g.
点评:本题考查元素化合物推断、化学方程式有关计算,(2)中计算为易错题目,学生容易忽略参加反应的水.

练习册系列答案
相关题目
下列有关化学用语使用正确的是( )
A、质量数为35的氯原子:
| ||
B、BaSO4的电离方程式:BaSO4=Ba2++S
| ||
| C、乙烯的结构简式:C2H4 | ||
D、氯原子结构示意图: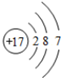 |