题目内容
下列事实中,能证明硫酸是强电解质的是( )
| A、用连有小灯泡的电路测硫酸溶液的导电性,灯泡较亮 |
| B、能跟锌反应产生氢气 |
| C、1mol/L硫酸溶液中H+浓度为2mol/L |
| D、能与碳酸钠反应放出二氧化碳气体 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:完全电离的电解质为强电解质,强酸、强碱和大部分的盐、金属氧化物等都是强电解质,如要证明硫酸为强酸,可判断能否完全电离,可根据硫酸和氢离子的物质的量浓度的关系进行判断.
解答:
解:题中硫酸与锌反应生成氢气以及与碳酸钠反应生成二氧化碳气体只能说明硫酸具有酸性,且酸性比碳酸强,但不能说明硫酸为强酸,导电性实验利用离子浓度大小确定导电性强弱,弱电解质当离子浓度较大灯泡也胡较亮,不能说明氯水是强电解质,而1 mol/L 硫酸溶液中H+ 浓度为2 mol/L,说明硫酸完全电离,为二元强酸.
故选C.
故选C.
点评:本题考查硫酸的性质,侧重于电解质的强弱的判断,注意把握实验设计的角度和可行性的评价,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构式为  ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A、苹果酸在一定条件下能发生酯化反应 |
| B、苹果酸在一定条件下能发生催化氧化反应 |
| C、苹果酸在一定条件下能发生加成反应 |
| D、1 mol苹果酸与Na2CO3溶液反应最多生成2 mol CO2 |
在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列有关说法不正确的是( )
| A、氢氧化铍是两性氢氧化物 |
| B、B、Si的电负性数值相似 |
| C、Li和Mg的原子半径相近,且核外电子排布相近 |
| D、铍与盐酸或氢氧化钠溶液反应均能产生气体 |
以下烃中,一氯代物只有一种的是( )
| A、CH3 CH2 CH2 CH2CH3 |
| B、CH3CH2CH3 |
| C、CH3CH2CH2CH3 |
| D、C(CH3)4 |
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3?10H2O的质量分别是( )
| A、1000mL,212g |
| B、950mL,543.4g |
| C、1000mL,572g |
| D、500mL,286g |
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.
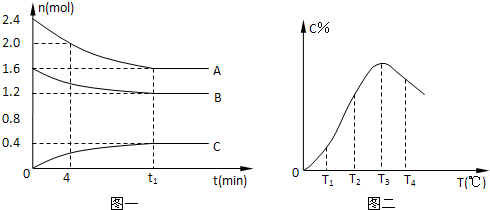
下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为吸热反应 |
下列有关化学用语使用正确的是( )
A、质量数为35的氯原子:
| ||
B、BaSO4的电离方程式:BaSO4=Ba2++S
| ||
| C、乙烯的结构简式:C2H4 | ||
D、氯原子结构示意图: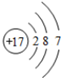 |
氢气、甲烷的热化学方程式分别为:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-89.3kJ?mol-1将氢气、甲烷按一定比例混合,所得气体密度是相同条件下氮气密度的一半,则9.8g该混合气体完全燃烧放出的热量为( )
| A、28.58kJ |
| B、82.16 kJ |
| C、53.58 kJ |
| D、89.3 kJ |