题目内容
下列各组物质分类正确的是( )
| 酸 | 碱 | 盐 | 氧化物 | |
| A | 硫酸 | 纯碱 | 石灰石 | 水 |
| B | 盐酸 | 烧碱 | 纯碱 | 生石灰 |
| C | 碳酸 | 胆矾 | 熟石灰 | 干冰 |
| D | 干冰 | 苛性钾 | 食盐 | 石灰石 |
| A、A | B、B | C、C | D、D |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:碱指电离时产生的阴离子全部都是氢氧根离子的化合物.酸指电离时产生的阳离子全部都是氢离子的化合物,盐指电离时生成金属阳离子(或NH4+)和酸根离子的化合物.酸性氧化物是指能与水作用生成酸或与碱作用生成盐和水的氧化物(且生成物只能有一种盐和水,不可以有任何其它物质生成).
解答:
解:A.纯碱是碳酸钠,属于盐不是碱;硫酸是酸;石灰石是碳酸钙,属于盐;水时不成盐氧化物,不是酸性氧化物,故A错误;
B.盐酸是酸;烧碱是氢氧化钠,属于碱;纯碱是碳酸钠,属于盐;生石灰是氧化钙,是氧化物,故B正确;
C.碳酸属于酸;胆矾是CuSO4?5H2O,属于盐不是碱,熟石灰是氢氧化钙,是碱不是盐;干冰是酸性氧化物,故C错误;
D.干冰是二氧化碳,不是酸;苛性钾是氢氧化钾,属于碱;食盐是混合物,不是盐;石灰石是碳酸钙,是盐而不属于酸性氧化物,故D错误;
故选B.
B.盐酸是酸;烧碱是氢氧化钠,属于碱;纯碱是碳酸钠,属于盐;生石灰是氧化钙,是氧化物,故B正确;
C.碳酸属于酸;胆矾是CuSO4?5H2O,属于盐不是碱,熟石灰是氢氧化钙,是碱不是盐;干冰是酸性氧化物,故C错误;
D.干冰是二氧化碳,不是酸;苛性钾是氢氧化钾,属于碱;食盐是混合物,不是盐;石灰石是碳酸钙,是盐而不属于酸性氧化物,故D错误;
故选B.
点评:本题考查物质的分类,了解常见物质的组成、物质的名称、分类,抓住各概念的特征进行分析判断是解答此类题的关键,属基础知识考查题,难度不大.

练习册系列答案
相关题目
已知:Cu+2Fe3+=Cu2++2Fe2+;Zn+2Fe3+=2Fe2++Zn2+.现将等物质的量的CuSO4、FeCl3和Zn于水中充分反应,所得混合物中除了SO42-、Cl-外,还含有( )
| A、Zn2+、Fe3+、Cu |
| B、Cu2+、Fe3+、Zn |
| C、Zn2+、Cu2+、Fe2+、Fe |
| D、Zn2+、Fe2+、Cu2+、Cu |
在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列有关说法不正确的是( )
| A、氢氧化铍是两性氢氧化物 |
| B、B、Si的电负性数值相似 |
| C、Li和Mg的原子半径相近,且核外电子排布相近 |
| D、铍与盐酸或氢氧化钠溶液反应均能产生气体 |
下列说法不正确的是( )
| A、电子云是笼罩在原子核外的云雾 |
| B、下列电子排布式:1s22s12p1是某原子基态的排布式 |
| C、任何能层中的d能级的轨道数都为5 |
| D、[Ar]3d64s2表示的是Fe原子的电子排布式 |
以下烃中,一氯代物只有一种的是( )
| A、CH3 CH2 CH2 CH2CH3 |
| B、CH3CH2CH3 |
| C、CH3CH2CH2CH3 |
| D、C(CH3)4 |
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3?10H2O的质量分别是( )
| A、1000mL,212g |
| B、950mL,543.4g |
| C、1000mL,572g |
| D、500mL,286g |
下列有关化学用语使用正确的是( )
A、质量数为35的氯原子:
| ||
B、BaSO4的电离方程式:BaSO4=Ba2++S
| ||
| C、乙烯的结构简式:C2H4 | ||
D、氯原子结构示意图: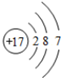 |