题目内容
8.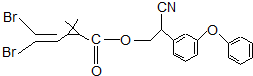 拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )
拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )| A. | 属于芳香族化合物 | B. | 属于卤代烃 | ||
| C. | 含有官能团酯基 | D. | 在一定条件下可以发生加成反应 |
分析 该分子中含有碳碳双键、酯基、苯环和醚键,具有烯烃、酯、苯、醚等物质的性质,能发生加成反应、还原反应、氧化反应、取代反应、水解反应等,据此分析解答.
解答 解:A.含有苯环,属于芳香化合物,故A正确;
B.该物质中含有Br、O、N元素,所以不属于卤代烃,故B错误;
C.含有酯基,具有酯类化合物的性质,可发生水解反应,故C正确;
D.含有碳碳双键和苯环,可发生加成反应,故D正确.
故选B.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,侧重考查烯烃、苯、醚及酯的性质,题目难度不大.

练习册系列答案
相关题目
18.下列各组微粒中,半径前者小于后者的是( )
| A. | C、O | B. | N、P | C. | Mg、Al | D. | Na、Na+ |
16.某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
(4)实验结论:同一周期主族元素从左到右失电子能力减弱,得电子能力增强.
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E生成淡黄色沉淀 |
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
20.下列表达式中错误的是( )
| A. | 过氧化氢的电子式: | B. | S2-的结构示意图: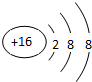 | ||
| C. | 氟化钙的电子式: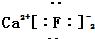 | D. | CO2分子的结构式:O=C=O |
17.12.8gCu与足量浓硝酸反应,铜完全反应后,如果NO3-减少0.22mol,则消耗硝酸的物质的量为( )
| A. | 0.22mol | B. | 0.40mol | C. | 0.42mol | D. | 0.62mol |
18.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
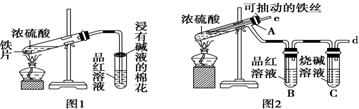
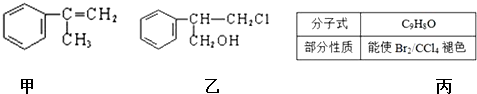
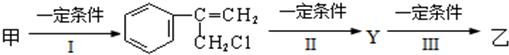
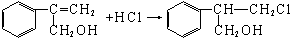 (不需注明反应条件).
(不需注明反应条件).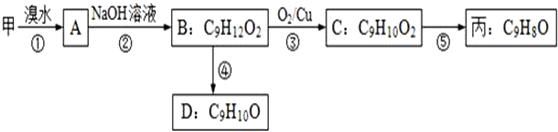
 .
. 、
、
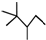 C8H18;
C8H18;  C6H12;
C6H12;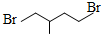 C5H10Br2;
C5H10Br2; 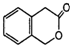 C9H8O2.
C9H8O2.