题目内容
17.12.8gCu与足量浓硝酸反应,铜完全反应后,如果NO3-减少0.22mol,则消耗硝酸的物质的量为( )| A. | 0.22mol | B. | 0.40mol | C. | 0.42mol | D. | 0.62mol |
分析 先根据n=$\frac{m}{M}$计算出铜的物质的量,反应消耗的硝酸分为两部分,一部分生成了硝酸铜,另一部分生成氮的氧化物,导致硝酸根离子浓度减小,据此结合质量守恒定律计算出消耗硝酸的总物质的量.
解答 解:12.8g铜的物质的量为:$\frac{12.8g}{64g/mol}$=0.2mol,由于铜完全反应,则反应生成硝酸铜的物质的量为0.2mol,生成硝酸铜消耗硝酸的物质的量为:0.2mol×2=0.4mol;
反应消耗的硝酸中,一部分生成氮的氧化物,单质硝酸根离子浓度减小,另一部分生成硝酸铜,硝酸根离子浓度不变,
所以消耗硝酸的总物质的量为:0.4mol+0.22mol=0.62mol,
故选D.
点评 本题考查了离子方程式的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
7.C、CO、CH4、C2H5OH是常用的燃料,它们每1g分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为32.8kJ、10.1kJ、55.6kJ、29.7kJ.相同物质的量的这四种燃料,完全燃烧时放出热量最少的是( )
| A. | C | B. | CO | C. | CH4 | D. | C2H5OH |
8.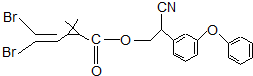 拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )
拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )
 拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )
拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图.下列对该化合物叙述不正确的是( )| A. | 属于芳香族化合物 | B. | 属于卤代烃 | ||
| C. | 含有官能团酯基 | D. | 在一定条件下可以发生加成反应 |
5.下列说法正确的是( )
| A. | 可用蘸有浓盐酸的棉棒检验输送氨气的管道是否漏气 | |
| B. | 氯水、氨水、浓硝酸都要存放在棕色瓶里 | |
| C. | 铵态氮肥不能与草木灰混合使用,但可以暴晒在太阳底下 | |
| D. | SO2具有漂白性,故可使酸性KMnO4溶液褪色 |
12.化学反应中,在一定条件(如加热)下有时仍存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中属于这种情况的是( )
①过量的Zn与浓硫酸溶液反应
②过量的二氧化锰与浓盐酸反应
③过量的铜与浓硫酸反应
④过量的铜与稀硝酸反应
⑤常温下过量浓硫酸与铝反应.
①过量的Zn与浓硫酸溶液反应
②过量的二氧化锰与浓盐酸反应
③过量的铜与浓硫酸反应
④过量的铜与稀硝酸反应
⑤常温下过量浓硫酸与铝反应.
| A. | ②③⑤ | B. | ②③④ | C. | ①④⑤ | D. | ①②③④⑤ |
2.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 蔗糖溶于水 | D. | SO2气体溶于水 |
9.下列事实中,可以证明Al2O3中一定存在离子键的是( )
| A. | 易溶于水 | B. | 有较高的熔点 | C. | 熔化时能导电 | D. | 水溶液能导电 |
6.下列有关烷烃的叙述中,不正确的是( )
| A. | 烷烃分子中,所有的化学键都是单键 | |
| B. | 烷烃在光照条件下都能与氯气发生取代反应 | |
| C. | 烷烃的分子通式为CnH2n+2,符合通式的烃不一定是烷烃 | |
| D. | 随着碳原子数的增加,烷烃的熔沸点逐渐升高 |
4.在硫酸的工业制法中,下列生产操作及对采取此操作的主要原因的叙述都正确的是( )
| A. | 硫铁矿燃烧前需要粉碎,因为大块的不能在空气燃烧 | |
| B. | 沸腾炉出来的炉气需净化,因为其中的SO2会与杂质反应 | |
| C. | SO2氧化为SO3时,使用催化剂可以提高硫酸的产率 | |
| D. | SO3用98.3%的浓硫酸吸收,目的是防止形成酸雾,以使SO3吸收完全 |