��Ŀ����
18�������⻯��--��������Ҫ�Ļ���ԭ�ϣ��ڹ�ũҵ�������й㷺��Ӧ�ã��������е�NO2�����ѳ�����������������ŷţ�
��1���ϳɰ�ԭ��������һ���Ʊ���ӦΪ��CO+H2O��g���TCO2+H2
��t��Cʱ����1L�ܱ������г���0.2molCO��0.3molˮ��������Ӧ����ƽ�����ϵ��c��H2��=0.12mol•L-1�����¶��´˷�Ӧ��ƽ�ⳣ��K=1�����������
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO������Ӧ���½���ƽ��ʱ��ˮ��������ת���ʦ���H2O��=50%��
��2��NH3��O2�ڲ�ϵ���������´�145��C�Ϳ�ʼ��Ӧ��4NH3��g��+5O2��g���T4NO��g��+6H2O��g����
��H=-905kJ•mol-1
��ͬ�¶���NO������ͼ1��ʾ���¶ȸ���900��Cʱ��NO�����½���ԭ���¶ȸ���900��ʱ��ƽ�������ƶ���
��3����֪��CH4��g��+2O2�TCO2��g��+2H2O����H=-890.3kJ•mol-1
N2��g��+O2��g���T2NO��g������H=+180kJ•mol-1
CH4���������������Ȼ�ѧ����ʽΪCH4��g��+4NO��g���TCO2��g��+2N2��g��+2H2O��l����H=-1250.3 kJ•mol-1��
��4����NO2��O2������NaNO2��ɵ�ȼ�ϵ��װ����ͼ2��ʾ����ʹ�ù�����ʯī��缫��Ӧ����һ��������Y���йص缫��Ӧ�ɱ�ʾΪNO2+NO3--e-=N2O5��
���� ��1������������ʽ�����ƽ��ʱ�����ʵ�����ƽ��Ũ�ȣ�����ƽ�ⳣ������ʽ���㣮
�ڱ����¶Ȳ��䣬ƽ�ⳣ�����䣮������ƽ����ϵ���ټ���0.1mol CO�����Ե�ЧΪ��ʼ����0.3molCO��0.3molH2O��
��μӷ�Ӧ��ˮ�����ʵ���Ϊxmol����������ʽ��x��ʾ�������ʵ�Ũ�ȱ仯����ƽ��ʱ�����ʵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������xֵ��������ת���ʶ�����㣻
��2�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ���
��3����֪����CH4��g��+2O2��g���TCO2��g��+2H2O��l������H=-890.3kJ•mol-1
��N2��g��+O2��g���T2NO��g������H=+180kJ•mol-1
���ݸ�˹���ɣ���-2���ڵ�CH4��g��+4NO��g���TCO2��g��+2N2��g��+2H2O��l�����ɼ��㷴Ӧ�ȣ�
��4��ȼ�ϵ�صĸ����Ϸ���ȼ��ʧȥ���ӵ�������Ӧ����NO2+NO3--e-=N2O5��
��� �⣺��1���ٶ��ڿ��淴Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ���ʵ���Ũ�ȣ�mol/L�� 0.2 0.3 0 0
ת�����ʵ���Ũ�ȣ�mol/L�� 0.12 0.12 0.12 0.12
ƽ�����ʵ���Ũ�ȣ�mol/L�� 0.08 0.18 0.12 0.12
���Ը��¶��´˷�Ӧ��ƽ�ⳣ��K=$\frac{0.12��0.12}{0.08��0.18}$=1��
�ʴ�Ϊ��1��
�ڱ����¶Ȳ��䣬ƽ�ⳣ�����䣬������ƽ����ϵ���ټ���0.1mol CO�����Ե�ЧΪ��ʼ����0.3molCO��0.3molH2O��
���ڿ��淴Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ���ʵ���Ũ�ȣ�mol/L�� 0.3 0.3 0 0
ת�����ʵ���Ũ�ȣ�mol/L�� x x x x
ƽ�����ʵ���Ũ�ȣ�mol/L�� 0.3-x 0.3-x x x
����$\frac{x•x}{��0.3-x��•��0.3-x��}$=1�����x=1.5
���Ե���Ӧ���½���ƽ��ʱ��ˮ��������ת���ʦ���H2O��=$\frac{1.5mol}{0.3mol}$��100%=50%��
�ʴ�Ϊ��50%��
��2�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ����������IJ��ʼ�С��
�ʴ�Ϊ���¶ȸ���900��ʱ��ƽ�������ƶ���
��3����֪����CH4��g��+2O2��g���TCO2��g��+2H2O��l������H=-890.3kJ•mol-1
��N2��g��+O2��g���T2NO��g������H=+180kJ•mol-1
���ݸ�˹���ɣ���-2���ڵ�CH4��g��+4NO��g���TCO2��g��+2N2��g��+2H2O��l������H=-890.3kJ•mol-1-2����+180kJ•mol-1��=-1250.3 kJ•mol-1��
�ʴ�Ϊ��CH4��g��+4NO��g���TCO2��g��+2N2��g��+2H2O��l����H=-1250.3 kJ•mol-1��
��4��ȼ�ϵ�صĸ����Ϸ���ȼ��ʧȥ���ӵ�������Ӧ����NO2+NO3--e-=N2O5���ʴ�Ϊ��NO2+NO3--e-=N2O5��
���� ���⿼���Ϊ�ۺϣ��漰��˹���ɵ�Ӧ�á���ѧƽ��ļ��㡢���ԭ����Ӧ�á�������ԭ��Ӧ��ͼ��ķ�����Ӧ�õȣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Լ��Ի���֪ʶ���ۺ�Ӧ����������Ŀ�Ѷ��еȣ�

| A�� | ������ú̿����ȡů���������γ��ޱ�Ȼ��ϵ | |
| B�� | ʳƷ��װ���г��˵����ɷ��� | |
| C�� | ���������п�ɷ�ֹ���ĸ�ʴ | |
| D�� | ���յع�������������ͷ��ϻ���������Ҫ�� |
 ���������Ǵ�����Ⱦ��֮һ��Ŀǰ��������������ķ����ж��֣�
���������Ǵ�����Ⱦ��֮һ��Ŀǰ��������������ķ����ж��֣������ԭ�����������������ڰ�װ�Ĵ�ת��������ʹβ������Ҫ��Ⱦ��ת��Ϊ�����ʣ���Ҫ��Ӧ���£���2NO��g��+2CO��g��?N2��g��+2CO2��g��
��1����֪��N2��g��+O2��g��?2NO��g����H=+180kJ•mol-1
| ��ѧ�� | O�TO | C�TO | C��O |
| ���ܣ�Kj/moL�� | 497 | 803 | 1072 |
��2����һ���¶��£������Ϊ1L���ܱ�������ͨ��2molNO��1molCO��10����ʱ��Ӧ2NO��g��+2CO��g��?N2��g��+2CO2��g���ﵽƽ��״̬����Ӧ�����з�Ӧ��Ũ����ʱ��仯�����ͼ��ʾ��
��ǰ10�������õ�����ʾ�ķ�Ӧ����Ϊ0.02mol?L-1?min-1��������¶��·�Ӧ��ƽ�ⳣ��KΪ$\frac{0.2��0��{4}^{2}}{1��{6}^{2}��0��{6}^{2}}$L?mol-1����ֻ����ʽ����Ҫ���������
���������¶Ȳ��䣬��15����ʱ���������ٴγ���NO1.6mol��CO20.4mol�����ʱ��Ӧ�Ħ���=���������������=��������
�����£�NO$��_{��Ӧ��}^{ClO_{2}}$ NO2$��_{��Ӧ��}^{Na_{2}SO_{3}ˮ��Һ}$N2����֪��Ӧ��Ļ�ѧ����ʽΪ2NO+ClO2+H2O=NO2+HNO3+HCl����Ӧ��Ļ�ѧ����ʽ��2NO2+4Na2SO3�TN2+4Na2SO4��
������11.2L N2����״������������ClO267.5g��
| A�� | �����������ֹ����ţ������������ܷ���������Ӧ | |
| B�� | ��������ʹ���Ը��������Һ����ˮ��ɫ�����ǵķ�Ӧԭ����ͬ | |
| C�� | ��������ͨ�����ַ�ʽ�ķ�Ӧ�������ָ߷������� | |
| D�� | 1mol�������ܹ�����2mol������ͬʱ�ų�1mol���� |
| �л��� | �������� | ������Һ | ����������ͭ | ������ |
| A | �����кͷ�Ӧ | ����Ӧ | �ܽ� | �ų����� |
| B | ����Ӧ | ����������Ӧ | ���ɺ�ɫ���� | �ų����� |
| C | ����Ӧ | ����������Ӧ | ���ɺ�ɫ���� | ����Ӧ |
| D | ����ˮ�ⷴӦ | ����Ӧ | ����Ӧ | ����Ӧ |
A��CH3CH2COOH��B��CH3CHOHCHO��C��HCOOCH2CH3��D��CH3COOCH3��
| �� ���� | IA | 0 | ||||||
| 1 | �� | IIA | IIIA | ��A | VA | ��A | VIIA | |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | |||
��2���õ���ʽ��ʾ�ߵ���̬�⻯����γɹ���
 ��
����3���ۡ��ܡ�����ԭ�Ӱ뾶�ɴ�С��˳����Na��S��F����Ԫ�ط��ţ�
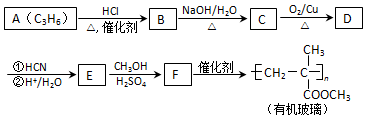
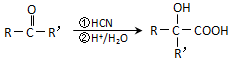 ��ע��R�������������Ҳ������Hԭ�ӣ�
��ע��R�������������Ҳ������Hԭ�ӣ�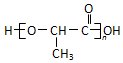 ����һ������ɽ�����ϣ��ο�������Ϣ������Ҵ��Ʊ�������ĺϳ�·��
����һ������ɽ�����ϣ��ο�������Ϣ������Ҵ��Ʊ�������ĺϳ�·��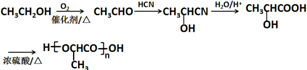 ����ʾ������Ӧ����X$\stackrel{��Ӧ����1}{��}$Y$\stackrel{��Ӧ����2}{��}$Z ����
����ʾ������Ӧ����X$\stackrel{��Ӧ����1}{��}$Y$\stackrel{��Ӧ����2}{��}$Z ����