题目内容
10.某有机物的结构简式为HOOC-CH=CH-CH2OH,关于该有机物下列说法错误的是( )| A. | 该物质有三种官能团,该物质自身能发生酯化反应 | |
| B. | 该物质能使酸性高锰酸钾溶液和溴水褪色,它们的反应原理相同 | |
| C. | 该物质能通过两种方式的反应生成两种高分子物质 | |
| D. | 1mol该物质能够消耗2mol金属钠同时放出1mol氢气 |
分析 有机物含有羧基,可发生中和、酯化反应,含有羟基,可发生取代、氧化反应,含有碳碳双键,可发生加成、加聚和氧化反应,以此解答该题.
解答 解:A.含有羧基、碳碳双键、羟基三种官能团,可自身发生酯化反应,故A正确;
B.含有碳碳双键,可被高锰酸钾氧化,与溴水发生加成反应,原理不同,故B错误;
C.含有碳碳双键,可发生加聚反应,含有羧基、羟基,可发生缩聚反应,故C正确;
D.含有羧基、羟基,则1mol该物质能够消耗2mol金属钠同时放出1mol氢气,故D正确.
故选B.
点评 本题考查有机物的结构和性质,侧重考查官能团的判断、物质的性质等知识点,为高考常见题型,难度不大,结构决定性质,性质体现结构,熟记官能团的性质是解题的关键,

练习册系列答案
相关题目
9.X、Y、Z、W是短周期主族元素,X原子最外层电子数是其内层电子数的3倍;Y的原子序数是其最外层电子数的6倍;Z的一种单质是自然界中最硬的物质;自然界中,W的单质多出现在火山口附近,且为淡黄色晶体.下列叙述正确的是( )
| A. | 原子半径的大小:Z>X>Y | |
| B. | Z的氢化物的沸点一定比X 的低 | |
| C. | W的最高价氧化物对应水化物的酸性在同主族中最强 | |
| D. | Y的单质与Z、X形成的化合物反应可冶炼金属 |
1.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)△H,所得实验数据如下表.
(1)实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,v(N)=0.001mol/(L•min);
(2)实验②中,该反应的平衡常数K=1;
(3)实验③中,此时化学反应速率是v(正)<v(逆)(填“=”、“>”或“<”);
(4)反应热△H<0(填“>”或“<”);
(5)应用化学反应速率与化学平衡原理解决化工生产实际问题,你认为下列说法不正确的是c(填字母序号).
a.化学反应速率理论可以指导怎样在一定时间内快出产品
b.勒夏特列原理可以指导怎样使有限原料多出产品
c.催化剂的使用是提高产品产率的有效办法
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
| 实验 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |||
| n(X) | n(Y) | n(M) | n(N) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0 | 0 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0 | 0 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | 0.25 | 0.25 | a |
(2)实验②中,该反应的平衡常数K=1;
(3)实验③中,此时化学反应速率是v(正)<v(逆)(填“=”、“>”或“<”);
(4)反应热△H<0(填“>”或“<”);
(5)应用化学反应速率与化学平衡原理解决化工生产实际问题,你认为下列说法不正确的是c(填字母序号).
a.化学反应速率理论可以指导怎样在一定时间内快出产品
b.勒夏特列原理可以指导怎样使有限原料多出产品
c.催化剂的使用是提高产品产率的有效办法
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
15.下列判断错误的是( )
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:Li>Na>K>Rb>Cs | ||
| C. | 酸性:HClO4>H2SO4>H2SeO4 | D. | 碱性:KOH>Mg(OH)2>Al(OH)3 |
19.表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述不正确的是( )
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6.-2 | -1 | -1 |
| A. | 气态氢化物的稳定性HG>HF>H2E | |
| B. | B2+、D3+、E2-、G-四种离子的核外电子排布相同 | |
| C. | A、E元素与氧元素可以形成三种常见的含氧酸盐 | |
| D. | C元素的原子最外层电子数等于电子层数 |
20.下列有关电解质溶液的说法不正确的是( )
| A. | 向Na2CO3溶液中通入NH3,$\frac{c(N{a}^{+})}{c(C{{O}_{3}}^{2-})}$减小 | |
| B. | 将0.1mol•L-1的K2C2O4溶液从25℃升温至35℃,$\frac{c({K}^{+})}{c({C}_{2}{{O}_{4}}^{2-})}$增大 | |
| C. | 向0.1mol•L-1的HF溶液中滴加NaOH溶液至中性,$\frac{c(N{a}^{+})}{c({F}^{-})}$=1 | |
| D. | 向0.1mol•L-1的CH3COONa溶液中加入少量水,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}$增大 |

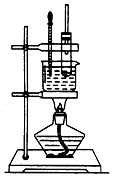 实验室制备硝基苯的实验装置如图所示,填写下列空白:
实验室制备硝基苯的实验装置如图所示,填写下列空白: