题目内容
一系列物质:NaCl、Cl2、NaClO、Cl2O5、HClO4是按某一规律排列的,下列组合中也完全照此规律排列的是( )
| A、Na2CO3 C CO2 CO NaHCO3 |
| B、Na2S S SO2 Na2SO3 Na2SO4 |
| C、NH4Cl N2 NaNO2 NO2 HNO3 |
| D、P2O5 H3PO4 Na3PO4 Na2HPO4 NaH2PO4 |
考点:根据化学式判断化合价
专题:氧化还原反应专题
分析:NaCl、Cl2、NaClO、Cl2O5、HClO4是按某氯元素的化合价逐渐增大这一规律排列的,分析每个选项中元素的化合价,得出正确结论.
解答:
解:NaCl、Cl2、NaClO、Cl2O5、HClO4是按某氯元素的化合价逐渐增大这一规律排列的,
A.Na2CO3中碳的化合价为+4价,C的化合价为0价,CO2中碳的化合价为+4价,CO中碳的化合价为+2价,NaHCO3中碳的化合价为+4价,不符合这一规律,故A错误;
B.Na2S中硫的化合价为-2价,S的化合价为0价,SO2中硫的化合价为+4价,Na2SO3中硫的化合价为+4价,Na2SO4中硫的化合价为+6价,不符合这一规律,故B错误;
C.NH4Cl中氮的化合价为-3价,N2中氮的化合价为0价,NaNO2中氮的化合价为+3价,NO2中氮的化合价为+4价,HNO3中氮的化合价为+5价,符合这一规律,故C正确;
D.P2O5中磷的化合价为+5价,H3PO4中磷的化合价为+5价,Na3PO4中磷的化合价为+5价,Na2HPO4中磷的化合价为+5价,NaH2PO4中磷的化合价为+5价,不符合这一规律,故D错误;
故选C.
A.Na2CO3中碳的化合价为+4价,C的化合价为0价,CO2中碳的化合价为+4价,CO中碳的化合价为+2价,NaHCO3中碳的化合价为+4价,不符合这一规律,故A错误;
B.Na2S中硫的化合价为-2价,S的化合价为0价,SO2中硫的化合价为+4价,Na2SO3中硫的化合价为+4价,Na2SO4中硫的化合价为+6价,不符合这一规律,故B错误;
C.NH4Cl中氮的化合价为-3价,N2中氮的化合价为0价,NaNO2中氮的化合价为+3价,NO2中氮的化合价为+4价,HNO3中氮的化合价为+5价,符合这一规律,故C正确;
D.P2O5中磷的化合价为+5价,H3PO4中磷的化合价为+5价,Na3PO4中磷的化合价为+5价,Na2HPO4中磷的化合价为+5价,NaH2PO4中磷的化合价为+5价,不符合这一规律,故D错误;
故选C.
点评:本题考查元素化合价的判断,难度不大.要注意掌握常见元素的化合价.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是( )
| A、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| B、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
短周期元素W、X、Y的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质.根据以上叙述,下列说法中一定正确的是( )
| A、上述四种元素的原子半径大小为Y<X<W |
| B、W、X、Y原子的核外最外层电子数的总和为10 |
| C、由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
| D、W与Y可形成既含极性共价键又含非极性共价键的化合物 |
在标准状况下,a g气体A与b g气体B的分子数相同,则正确的是( )
| A、气体A和气体B的摩尔质量之比为b:a |
| B、同温同压下,气体A和气体B的密度之比为b:a |
| C、质量相同的气体A与气体B的分子数之比为a:b |
| D、相同状况下,同体积的气体A与气体B的质量之比为a:b |
下列电离方程式错误的是( )
| A、NaHCO3═Na++H++CO32- |
| B、NaHSO4═Na++H++SO42- |
| C、FeCl3═Fe3++3Cl- |
| D、Ba(OH)2═Ba2++2OH- |
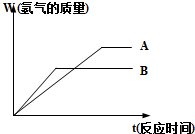 等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:
等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示: