题目内容
在标准状况下,a g气体A与b g气体B的分子数相同,则正确的是( )
| A、气体A和气体B的摩尔质量之比为b:a |
| B、同温同压下,气体A和气体B的密度之比为b:a |
| C、质量相同的气体A与气体B的分子数之比为a:b |
| D、相同状况下,同体积的气体A与气体B的质量之比为a:b |
考点:物质的量的相关计算
专题:计算题
分析:ag气体A和bg气体B所含分子数相等,则物质的量相等,二者的摩尔质量之比为a:b,结合n=
=
,ρ=
=
=
解答该题.
| m |
| M |
| N |
| NA |
| m |
| V |
| nM |
| nVm |
| M |
| Vm |
解答:
解:A.ag气体A和bg气体B所含分子数相等,则物质的量相等,二者的摩尔质量之比为a:b,故A错误;
B.结合ρ=
=
=
可知,同温、同压下,气体A和气体B的密度之比等于摩尔质量之比为a:b,故B错误;
C.由n=
=
,相同质量时气体的分子数之比与摩尔质量呈反比,则相同质量的气体A和气体B的分子数之比为b:a,故C错误;
D.相同状况下,同体积的气体A与气体B,物质的量相等,根据m=nM,则相同体积的气体A和气体B的质量之比为a:b,故D正确;
故选D.
B.结合ρ=
| m |
| V |
| nM |
| nVm |
| M |
| Vm |
C.由n=
| m |
| M |
| N |
| NA |
D.相同状况下,同体积的气体A与气体B,物质的量相等,根据m=nM,则相同体积的气体A和气体B的质量之比为a:b,故D正确;
故选D.
点评:本题综合考查物质的量的相关计算,侧重于学生的分析能力和计算能力的考查,为高考常见题型,题目难度中等,注意把握相关计算公式的运用.

练习册系列答案
相关题目
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O═7X+5FeSO4+12H2SO4,下列说法正确的是( )
| A、X的化学式为CuS,它既是氧化产物又是还原产物 |
| B、5 mol FeS2发生反应,有10 mol电子转移 |
| C、产物中的SO42-离子有一部分是氧化产物 |
| D、FeS2只作还原剂 |
人们利用纳米级(1~100nm,1nm=10-9m)粒子物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用.将纳米级粒子物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述不正确的是( )
| A、该分散系能产生丁达尔效应 |
| B、该分散质颗粒能透过滤纸 |
| C、该分散质颗粒能透过半透膜 |
| D、该分散质颗粒能发生布朗运动 |
一系列物质:NaCl、Cl2、NaClO、Cl2O5、HClO4是按某一规律排列的,下列组合中也完全照此规律排列的是( )
| A、Na2CO3 C CO2 CO NaHCO3 |
| B、Na2S S SO2 Na2SO3 Na2SO4 |
| C、NH4Cl N2 NaNO2 NO2 HNO3 |
| D、P2O5 H3PO4 Na3PO4 Na2HPO4 NaH2PO4 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1molCl2与足量的氢氧化钠溶液反应转移的电子数为0.2 NA |
| B、12.5mL 16mol/L浓硫酸与足量铜反应,转移的电子数为0.2NA |
| C、6.2g氧化钠和7.8g过氧化钠中所含有的离子数均为0.3 NA |
| D、2.24L氯气与氢氧化钠溶液完全反应转移的电子数为0.1 NA |
下列反应的离子方程式中,书写正确的是( )
| A、石英溶于氢氧化钠溶液:SiO2+2OH-═SiO32-+H2O |
| B、将铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、铁粉与硫酸铁溶液反应:Fe+Fe3+═2Fe2+ |
| D、金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
 A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大.
A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大.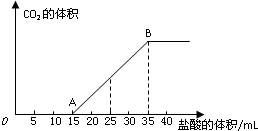 将一定体积的CO2通入到50mL某浓度的NaOH溶液中,得到溶液甲.为了测定其溶液甲的成分,向该溶液甲中加入1mol/L的盐酸,所加入的盐酸与产生CO2的体积(标况)的关系如图所示:
将一定体积的CO2通入到50mL某浓度的NaOH溶液中,得到溶液甲.为了测定其溶液甲的成分,向该溶液甲中加入1mol/L的盐酸,所加入的盐酸与产生CO2的体积(标况)的关系如图所示: