题目内容
室温下,下列各组离子在指定溶液中能大量共存的( )
A、pH=1的溶液中K+ CrO
| ||||||
B、饱和氯水中Cl- NO
| ||||||
C、能使pH试纸变红的溶液NH
| ||||||
D、FeCl2溶液中K+ Na+ SO
|
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液,显酸性,CrO42-转化为Cr2O72-;
B.饱和氯水,含氯气等氧化性物质;
C.能使pH试纸变红的溶液,显酸性;
D.Fe2+、AlO2-相互促进水解.
B.饱和氯水,含氯气等氧化性物质;
C.能使pH试纸变红的溶液,显酸性;
D.Fe2+、AlO2-相互促进水解.
解答:
解:A.pH=1的溶液,显酸性,酸性溶液中CrO42-转化为Cr2O72-,不能大量共存,故A不选;
B.饱和氯水,含氯气等氧化性物质,与SO32-发生氧化还原反应,不能共存,故B不选;
C.能使pH试纸变红的溶液,显酸性,该组离子之间不反应,可大量共存,故C选;
D.Fe2+、AlO2-相互促进水解,不能大量共存,故D不选;
故选C.
B.饱和氯水,含氯气等氧化性物质,与SO32-发生氧化还原反应,不能共存,故B不选;
C.能使pH试纸变红的溶液,显酸性,该组离子之间不反应,可大量共存,故C选;
D.Fe2+、AlO2-相互促进水解,不能大量共存,故D不选;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,注意选项A、D为解答的难点,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某气体可能含有N2、HCl、CO中的一种或几种,将其依次通入足量NaHCO3溶液和灼热CuO,气体的体积都没有变化,再通过足量的碱石灰,气体体积减小,但还有剩余气体,以下对该气体组分判断正确的是( )
| A、一定没有N2,CO和HCl至少有1种 |
| B、一定有N2,HCl和CO |
| C、一定有N2,CO和HCl至少有1种 |
| D、一定有N2和CO,没有HCl |
某有机物结构简式如图所示(未表示出其空间构型).下列它的性质描述不正确的是( )
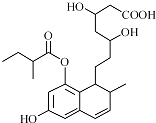

| A、能与FeCl3 溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加成、取代、消去反应 |
| D、1mol该物质最多可与3mol NaOH反应 |
几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | L | X | R | T |
| 原子半径/nm | 0.191 | 0.102 | 0.154 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
| A、L单质的熔点比R单质的高 |
| B、T对应的氢化物的沸点比X对应的氢化物高 |
| C、R单质在氧气中燃烧生成R2O2 |
| D、L、X形成的简单离子核外电子数相等 |
下列氧化还原反应中,实际参加反应的氧化剂与还原剂物质的量之比正确的是( )
①2H2S+SO2=3S+2H2O; 1:2
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 6:1
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Na2O2+2H2O=4NaOH+O2; 1:1.
①2H2S+SO2=3S+2H2O; 1:2
②6HNO3(浓)+S=H2SO4+6NO2+2H2O; 6:1
③Fe+4HNO3=Fe(NO3)3+NO+2H2O; 1:1
④2Na2O2+2H2O=4NaOH+O2; 1:1.
| A、只有①正确 |
| B、只有③ |
| C、只有①和④ |
| D、①②③④都正确 |
下列热化学方程式或离子方程式中,正确的是( )
| A、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| B、向Mg(HCO3)2溶液中加入过量的澄清石灰水:Mg2++2HCO3-+2OH一+Ca2+═MgCO3↓+CaCO3↓+2H2O |
| C、乙烯的燃烧热为akJ/mol(a>0),则乙烯燃烧的热化学方程式可表示为:C2H4(g)+3O2(g)═2CO2(g)+2H2O(g)△H=-akJ/mol |
| D、Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
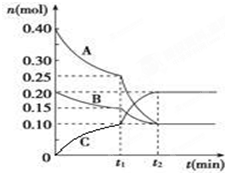 现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:
现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图: