题目内容
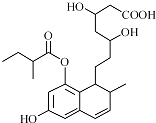
某有机物结构简式如图所示(未表示出其空间构型).下列它的性质描述不正确的是( )

| A、能与FeCl3 溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加成、取代、消去反应 |
| D、1mol该物质最多可与3mol NaOH反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含酚-OH、-COOC-、醇-OH、-COOH,结合酚、酯、醇、羧酸性质来解答.
解答:
解:A.含酚-OH,能与FeCl3 溶液发生显色反应,故A正确;
B.含酚-OH、醇-OH,能使酸性KMnO4溶液褪色,故B正确;
C.含苯环可发生加成反应,含-OH可发生取代、消去反应,故C正确;
D.酚-OH、-COOH、-COOC-均与NaOH反应,且-COOC-水解生成的酚-OH也反应,则1mol该物质最多可与4mol NaOH反应,故D错误;
故选D.
B.含酚-OH、醇-OH,能使酸性KMnO4溶液褪色,故B正确;
C.含苯环可发生加成反应,含-OH可发生取代、消去反应,故C正确;
D.酚-OH、-COOH、-COOC-均与NaOH反应,且-COOC-水解生成的酚-OH也反应,则1mol该物质最多可与4mol NaOH反应,故D错误;
故选D.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重醇、羧酸、酚、酯性质的考查,注重分析与应用能力的考查,选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol,下列叙述正确的是( )
| A、2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ |
| B、2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),吸收热量571.6 kJ |
| C、2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ |
| D、2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
下列有关化学反应速率的说法正确的是( )
| A、化学反应速率只能用一定时间内反应物浓度的减少来表示 |
| B、化学反应速率的大小主要取决于反应物的性质 |
| C、化学反应达到最大限度时,正逆反应速率也达到最大且相等 |
| D、用铁片和稀硫酸反应制取氢气时改用98%浓硫酸可以加快产生氢气的速率 |
下列表述正确的是( )
| A、将 0.1 mol?L-1HCl溶液加热到100℃,溶液的pH仍为1 |
| B、将pH=4的醋酸溶液加水稀释后,溶液中所有离子的浓度均降低 |
| C、若1mLpH=1的盐酸与10mLNaOH溶液混合后溶液的pH=7,则NaOH溶液的pH=12 |
| D、在滴有酚酞试液的氨水中,加入NH4Cl至溶液呈无色,此时溶液一定显中性 |
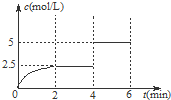 一定温度下有可逆反应:A(g)+2B(g)?2C(g)+D(g).现将4mol A和8mol B加入体积为2L的某密闭容器中,反应至4min时,改变某一条件,测得C的物质的量浓度随时间变化的曲线如图所示.下列有关说法中正确的是( )
一定温度下有可逆反应:A(g)+2B(g)?2C(g)+D(g).现将4mol A和8mol B加入体积为2L的某密闭容器中,反应至4min时,改变某一条件,测得C的物质的量浓度随时间变化的曲线如图所示.下列有关说法中正确的是( )| A、0~2 min内,正反应速率逐渐增大 |
| B、4 min时,A的转化率为50% |
| C、6 min时,B的体积分数为25% |
| D、4 min时,改变条件后,平衡向逆反应方向移动 |
8克铜与一定量浓硝酸完全反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与a L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.则a的值为( )
| A、2.8 L |
| B、1.4 L |
| C、3 L |
| D、4.2 L |
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则NaHSO4溶液的pH是(已知lg2=0.3)( )
| A、2 | B、2.3 |
| C、2.6 | D、2.9 |
室温下,下列各组离子在指定溶液中能大量共存的( )
A、pH=1的溶液中K+ CrO
| ||||||
B、饱和氯水中Cl- NO
| ||||||
C、能使pH试纸变红的溶液NH
| ||||||
D、FeCl2溶液中K+ Na+ SO
|
