题目内容
16.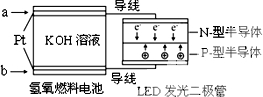 LED产品的使用为城市增添色彩.如图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
LED产品的使用为城市增添色彩.如图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )| A. | 该装置将化学能最终转化为电能 | |
| B. | a处通入O2 | |
| C. | b处为电池正极,发生还原反应 | |
| D. | 通入O2的电极上发生的电极反应为O2+4H++4e-=2H2O |
分析 A、该装置的能量转换是化学能为电能最终转化为光能;
B、由电子流向可知a为负极,b为正极,以此判断;
C、通氧气的一极为b极,b为正极发生的电极反应为O2+2H2O+4e-═4OH-;
D、碱性条件下,氧气得电子生成氢氧根离子.
解答 解:A、燃料电池中将化学能转化为电能,LED产品中电能转化为光能,所以该装置的能量转换是化学能为电能最终转化为光能,故A错误;
B、由电子流向可知a为负极,b为正极,负极上发生氧化反应,通入氢气,正极上发生还原反应,通入的是氧气,即b处通入O2,故B错误;
C、b为正极发生的电极反应为O2+2H2O+4e-═4OH-,氧气得电子发生还原反应,故C正确;
D、通氧气的一极为b极,碱性条件下,氧气得电子生成氢氧根离子,则b极发生的电极反应为O2+2H2O+4e-═4OH-,故D错误.
故选C.
点评 本题考查原电池知识,题目难度不大,本题注意根据图示电子的流向判断电源的正负极为解答该题的关键,侧重于考查学生对原电池原理的应用能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
7.纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体.下列区分这两种物质的方法正确的是( )
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 | |
| B. | 用洁净铁丝蘸取两种样品在酒精灯火焰上灼烧,火焰颜色呈黄色的是小苏打 | |
| C. | 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 | |
| D. | 先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
4.下列化学用语使用正确的组合是( )
①氘表示为12D
②乙炔的分子结构模型示意图:
③有机还原剂LiAlH4中,氢显-1价
④质量为40的钙原子:4020Ca
⑤NH4Cl的电子式: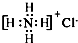
⑥2-甲基丁醇的结构简式: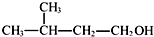
①氘表示为12D
②乙炔的分子结构模型示意图:

③有机还原剂LiAlH4中,氢显-1价
④质量为40的钙原子:4020Ca
⑤NH4Cl的电子式:
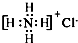
⑥2-甲基丁醇的结构简式:
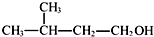
| A. | ①②③ | B. | ③④ | C. | ②④⑤ | D. | ①④⑥ |
1.下列说法正确的是( )
| A. | 新制的氯水保存在无色玻璃瓶中 | |
| B. | 氢气在氯气中燃烧生成白色烟雾 | |
| C. | 常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性 | |
| D. | 向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性 |
8.根据下图海水综合利用的工业流程图,判断下列说法正确的是
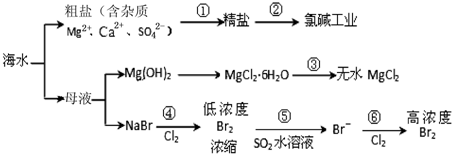
已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等( )

已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等( )
| A. | 除去粗盐中杂质(Mg2+、Ca2+、SO42-),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2 | |
| D. | 从第④步到第⑥步的目的是为了浓缩富集溴 |
5.分子式为C5H12O的醇与C4H8O2的羧酸在浓H2SO4存在时共热生成的酯有( )
| A. | 6种 | B. | 16种 | C. | 32种 | D. | 12种 |
11.短周期元素X、Y、Z、W在周期表中的相对位置如右图所示,已知它们的最外层电子数之和为21,下列说法错误的是( )


| A. | 原子半径由大到小的顺序:X、Y、Z、W | |
| B. | 元素最高正价由低到高的顺序:X、Y、Z、W | |
| C. | 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W | |
| D. | 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z |