题目内容
下列叙述中正确的是( )
| A、硝酸的摩尔质量63g |
| B、1mol CO的体积约为22.4L |
| C、2g氢气所含原子数目为1mol |
| D、铁的摩尔质量在数值上等于铁原子的相对原子质量 |
考点:物质的量的相关计算
专题:计算题
分析:A.硝酸的摩尔质量63g/mol;
B.CO不一定处于标况下,其所处状态的气体摩尔体积不一定是22.4L/mol;
C.氢原子质量为2g,根据n=
计算氢原子物质的量;
D.摩尔质量以g/mol为单位,数值上等于其相对分子质量.
B.CO不一定处于标况下,其所处状态的气体摩尔体积不一定是22.4L/mol;
C.氢原子质量为2g,根据n=
| m |
| M |
D.摩尔质量以g/mol为单位,数值上等于其相对分子质量.
解答:
解:A.1mol硝酸的质量为63g,硝酸的摩尔质量63g/mol,故A错误;
B.CO不一定处于标况下,温度、压强会影响其体积,其所处状态的气体摩尔体积不一定是22.4L/mol,1molCO的体积不一定是22.4L,故B错误;
C.氢原子质量为2g,氢原子物质的量为
=2mol,故C错误;
D.Fe的摩尔质量是56g/mol,等于其相对分子质量56,二者数值上相等,故D正确,
故选D.
B.CO不一定处于标况下,温度、压强会影响其体积,其所处状态的气体摩尔体积不一定是22.4L/mol,1molCO的体积不一定是22.4L,故B错误;
C.氢原子质量为2g,氢原子物质的量为
| 2g |
| 1g/mol |
D.Fe的摩尔质量是56g/mol,等于其相对分子质量56,二者数值上相等,故D正确,
故选D.
点评:本题考查物质的量有关计算、摩尔质量、气体摩尔体积,注意气体摩尔体积的使用体积与对象,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列热化学方程式正确的是( )
| A、2SO2+O2?2SO3;△H=-196.6 kJ?mol-1 | ||
B、H2 (g)+
| ||
| C、2H2 (g)+O2 (g)=2H2O(l);△H=-571.6 kJ | ||
| D、C(s)+O2 (g)=CO2 (g);△H=+393.5 kJ?mol-1 |
下列各项内容中,排列顺序正确的是( )
①氧化性:KMnO4>MnO2>Cl2
②单质的密度:Na<K<Rb
③微粒半径:K+>S2->F
④物质的熔点:Li>Na>K
⑤氢化物的沸点:H2Se>H2S>H2O.
①氧化性:KMnO4>MnO2>Cl2
②单质的密度:Na<K<Rb
③微粒半径:K+>S2->F
④物质的熔点:Li>Na>K
⑤氢化物的沸点:H2Se>H2S>H2O.
| A、①③ | B、②④ | C、①④ | D、③⑤ |
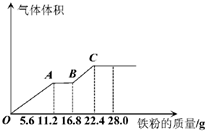 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析错误的是( )| A、AB段的反应为:Fe+2Fe3+=3Fe2+ |
| B、第二份溶液中最终溶质为FeSO4 |
| C、混合酸中NO3-物质的量为0.4mol |
| D、混合酸中H2SO4浓度为5mol?L-1 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4LCCl4中含有的分子数目为NA |
| B、16.8g铁粉与足量水蒸气完全反应转移电子数为0.9NA |
| C、已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.当该反应放出184.8kJ热量时,形成N-H键数为12NA |
| D、1mol乙烯和丙烯的混合气体中α键数为5NA |
下列溶液中,Cl-的物质的量浓度与50mL 1mol?L-1AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A、50 mL 1 mol?L-1KCl溶液 |
| B、25 mL 2 mol?L-1Ca(Cl)2溶液 |
| C、150 mL 3 mol?L-1KCl溶液 |
| D、50 mL 1 mol?L-1 MgCl2溶液 |
有A、B、C、D四个反应的焓变和熵变如表所示:下列说法正确的是( )
| 反应 | A | B | C | D |
| △H/kJ?mol-1 | 10.5 | 1.80 | -126 | -11.7 |
| △S/kJ?mol-1?k-1 | 30.0 | -113.0 | 84.0 | -105.0 |
| A、反应A在任何温度下均可自发进行 |
| B、反应B在任何温度下均不可自发进行 |
| C、反应C必须在温度高于170℃时才能自发进行 |
| D、反应D在任何温度下均不可自发进行 |