题目内容
1.2mol H2含有2NA个氢分子,4NA个氢原子4 mol H.分析 根据n=$\frac{N}{{N}_{A}}$,结合氢气的组成分析解答.
解答 解:2mol H2含有2NA 个氢分子,氢气是双原子分子,所以含4mol的氢原子,含4NA 氢原子,故答案为:2NA;4NA;4.
点评 本题考查物质的量的相关计算,学生要学会应用公式的同时,要结合物质的组成分析解答,比较容易.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
12.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 土壤胶体带负电荷,有利于铵态氮肥的吸收 | |
| B. | 加工后具有吸水性的植物纤维可用作食品干燥剂 | |
| C. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| D. | 燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
9.下列说法不正确的是( )
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 加热、蒸发MgCl2饱和溶液可得无水MgCl2晶体 | |
| C. | 工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 | |
| D. | 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
13.下列叙述正确的是( )
| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| C. | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率不改变快 |
10.把NaHCO3和Na2CO3•10H2O混合物5.38g溶于水制成100mL溶液,其中c(Na+)=0.4mol/L.如果把5.38g这种混合物加热至恒重所得固体的质量( )
| A. | 2.65g | B. | 2.12g | C. | 3.9g | D. | 4.65g |
 )和抗癫痫药物
)和抗癫痫药物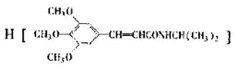 的路线如下(部分反应条件和试剂略去)
的路线如下(部分反应条件和试剂略去)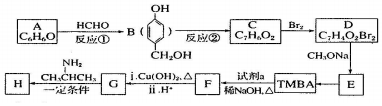
 +H2O(R、R′表示烃基或氢原子)
+H2O(R、R′表示烃基或氢原子)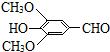 ,试剂a的分子式是C2H4O.
,试剂a的分子式是C2H4O. +2Br2→
+2Br2→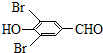 +2HBr.
+2HBr.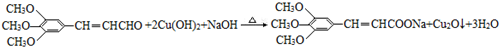 .
.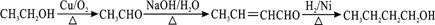 .
.