题目内容
10.把NaHCO3和Na2CO3•10H2O混合物5.38g溶于水制成100mL溶液,其中c(Na+)=0.4mol/L.如果把5.38g这种混合物加热至恒重所得固体的质量( )| A. | 2.65g | B. | 2.12g | C. | 3.9g | D. | 4.65g |
分析 固体混合物加热至恒重时,剩余固体为Na2CO3,根据Na元素守恒计算出剩余固体的物质的量,进而计算质量.
解答 解:固体混合物加热至恒重时,剩余固体为Na2CO3,
100mL溶液,其中c(Na+)═0.4mol•L-1.
则n(Na+)═0.1L×0.4mol•L-1=0.04mol,
n(Na2CO3)=0.02mol,
m(Na2CO3)=0.02mol×106g/mol=2.12g,
故选B.
点评 本题考查混合物的计算,题目难度不大,注意加热后剩余固体的成分,根据质量守恒计算.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
18.为了配制NH4+的浓度与Cl-的浓度之比为1:1的溶液,可在NH4Cl溶液中加入( )
| A. | 适量的HCl | B. | 适量的NaCl | C. | 适量的氨水 | D. | 适量的NaOH |
5.下列关于铵盐的叙述中正确的是( )
①所有铵盐都有氨的刺激性气味
②所有铵盐都溶于水
③铵盐不稳定,受热易分解
④铵盐能与碱反应,受热放出氨气
⑤铵盐都不能与酸反应.
①所有铵盐都有氨的刺激性气味
②所有铵盐都溶于水
③铵盐不稳定,受热易分解
④铵盐能与碱反应,受热放出氨气
⑤铵盐都不能与酸反应.
| A. | ①③④ | B. | ②③④ | C. | ①②③④ | D. | ①②③④⑤ |
15.二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域.已知二茂铁熔点是173℃(在100℃时开始升华),沸点是249℃,不溶于水,易溶于苯、乙醚等非极性溶剂.下列说法不正确的是( )
| A. | 二茂铁属于分子晶体 | |
| B. | 在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键 | |
| C. | 已知环戊二烯的结构式为: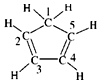 ,则其中仅有1个碳原子采取sp3杂化 ,则其中仅有1个碳原子采取sp3杂化 | |
| D. | C5H5-中一定含π键 |
2.W、X、Y、Z是原子序数依次增大的四种短周期元素,已知W的原子半径是所有元素中最小,四种元素的电子层数之和及最外层电子数之和均为10,且它们分别属于连续的四个主族.下列说法正确的是( )
| A. | W、X、Y元素的简单离子对水的电离平衡的影响是相同的 | |
| B. | 工业上获得X、Y单质的方法主要是电解其熔融的氯化物 | |
| C. | X、Y、Z的最高价氧化物对应的水化物两两之间能反应 | |
| D. | Y元素所形成的离子是其所在周期中半径最小的简单离子 |
20.从溴乙烷制取1,2-二溴乙烷,下列转化方案中最好的是( )
| A. | CH3CH2Br$→_{△}^{NaOH水溶液}$CH3CH2OH$→_{170℃}^{H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br$→_{醇溶液}^{NaOH}$CH2=CH2$\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br$\stackrel{NaOH}{→}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br |