题目内容
5.2016年环境日主题为“改善环境质量 推动绿色发展”,旨在动员引导社会各界着力践行人与自然和谐共生和绿色发展理念,从身边小事做起,共同履行环保责任,呵护环境质量,共建美丽家园.下列有关说法不正确的是( )| A. | 开发废旧电池综合利用技术,防止重金属盐对土壤水资源造成污染 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 倡导低碳生活,使用太阳能、风能等代替化石燃料,可减少温室气体的排放 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
分析 A.废旧电池中含有铅、镉、汞等重金属,能污染土壤和水资源;
B.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染;
C.“低碳生活”就是减少二氧化碳的排放,从而减缓温室效应;
D.垃圾是放错地方的资源,应分类回收利用.
解答 解:A.废旧电池中含有铅、镉、汞等重金属,开发废电池综合利用技术,防止其中重金属盐对土壤和水资源造成污染,符合可持续发展观念,故A正确;
B.对环境污染进行治理是对已经产生的污染治理,绿色化学又称环境友好化学,其核心就是要利用化学反应原理从源头消除污染,故B错误;
C.“低碳生活”就是通过各种手段、方法,尽量减少二氧化碳的排放,从而减缓温室效应,故C正确;
D.垃圾是放错地方的资源,应分类回收利用,故D正确;.
故选B.
点评 本题考查环境污染及治理,侧重于化学与人体健康的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列热化学方程式叙述正确的是( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol (燃烧热) | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | S(s)+O2(g)═SO2(g)△H=-296.8 kJ/mol (反应热) | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
16.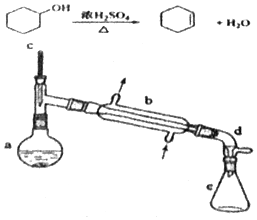 分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
可能用到的有关数据如下:
Ⅰ.合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1ml浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)分离提纯过程中加入无水氯化钙的目的是干燥.
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶.
 分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1ml浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)分离提纯过程中加入无水氯化钙的目的是干燥.
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶.
13.标准状况下,将1g氦气、11g二氧化碳和4g氧气混合,该混合气体的体积约为( )
| A. | 8.4 L | B. | 11.2 L | C. | 14.0 L | D. | 16.8 L |
10.用红色激光照射下列物质,能观察到丁达尔效应的是( )
| A. | 乙醇溶液 | B. | 氢氧化铁胶体 | C. | 酸酸铜溶液 | D. | 蔗糖溶液 |
14.可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A. | 分别加入碘化钾溶液,观察颜色变化 | |
| B. | 分别加热,观察是否生成沉淀 | |
| C. | 分别滴加浓硝酸 | |
| D. | 分别灼烧,闻味道 |
7. 实验室制取乙酸乙酯的主要步骤如下
实验室制取乙酸乙酯的主要步骤如下
①在25mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液.
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置分层.
④分离出乙酸乙酯层、洗涤、干燥.
以下数据可供参考:
按要求回答下列问题,
(1)配制该混合液试剂的添加顺序为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加冰醋酸.
(2)写出该反应的化学方程式:CH3COOH+CH3CH2OH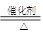 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
(3)该反应中哪些措施可以提高乙酸的转化率CD.
A.使用碎瓷片 B.酒精灯加热C.浓硫酸作吸水剂 D.将生成的乙酸乙酯蒸出
(4)上述实验中饱和碳酸钠溶液的主要是BCD(填字母)
A.加速酯的生成,提高其产率
B.降低乙酸乙酯的溶解度,便于液体分层
C.中和蒸出来的乙酸
D.吸收蒸出来的乙醇
(5)步骤②中需要小火均匀加热操作,其主要理由是:①温度过高可能发生其他副反应②减少乙酸乙醇的挥发.
(6)分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,通过洗涤出去碳酸钠、乙醇;为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.浓硫酸 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
 实验室制取乙酸乙酯的主要步骤如下
实验室制取乙酸乙酯的主要步骤如下①在25mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液.
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置分层.
④分离出乙酸乙酯层、洗涤、干燥.
以下数据可供参考:
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸 |
| 熔(℃) | -117.0 | 16.6 | -83.6 | ------ |
| 沸(℃) | 78.0 | 117.9 | 77.5 | 338.0 |
(1)配制该混合液试剂的添加顺序为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加冰醋酸.
(2)写出该反应的化学方程式:CH3COOH+CH3CH2OH
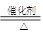 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.(3)该反应中哪些措施可以提高乙酸的转化率CD.
A.使用碎瓷片 B.酒精灯加热C.浓硫酸作吸水剂 D.将生成的乙酸乙酯蒸出
(4)上述实验中饱和碳酸钠溶液的主要是BCD(填字母)
A.加速酯的生成,提高其产率
B.降低乙酸乙酯的溶解度,便于液体分层
C.中和蒸出来的乙酸
D.吸收蒸出来的乙醇
(5)步骤②中需要小火均匀加热操作,其主要理由是:①温度过高可能发生其他副反应②减少乙酸乙醇的挥发.
(6)分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,通过洗涤出去碳酸钠、乙醇;为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.浓硫酸 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
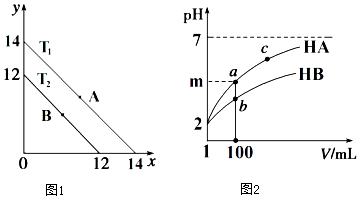 (1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.
(1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.