题目内容
19.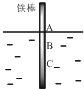 将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )
将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )| A. | 铁棒AB段发生反应为O2+4e-+2H2O=4OH- | |
| B. | 腐蚀过程中在铁棒上会产生微电流,且方向是AB段到BC段 | |
| C. | 向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 | |
| D. | 产生这种现象的本质原因是铁棒所处的化学环境不同 |
分析 铁板在水溶液中发生吸氧腐蚀,属于原电池,BC段作原电池负极、AB段作原电池正极,据此解答即可.
解答 解:铁板在水溶液中发生吸氧腐蚀,属于原电池,BC段作原电池负极、AB段作原电池正极,
A、依据分析可知,AB段为原电池的正极,发生反应O2+4e-+2H2O=4OH-,故A正确;
B、腐蚀过程中BC段为原电池的负极,在此生成微电流,电子从BC流向AB,故电流方向为从AB到BC,故B正确;
C、向水中加入一定量的硫酸钾后,电解质溶液中离子浓度升高,化学反应速率加快,故C错误;
D、此原电池的构成是由于铁棒所处的化学环境不同,故D正确,故选C.
点评 本题考查金属的吸氧腐蚀,明确各个电极上发生的反应及离子移动方向即可解答,会正确书写电极反应式,知道铁锈的成分,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
9.下列实验中,实验操作、现象及结论都正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 向某溶液中滴加BaCl2溶液和稀HNO3 | 产生白色沉淀 | 溶液中一定含有SO42- |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 向盛有0.5mol•L-1Fe(NO3)2溶液的试管中加入0.5mol•L-3H2SO4溶液 | 在试管口处现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液呈紫色 | 原溶液中有I- |
| A. | A | B. | B | C. | C | D. | D |
10.某有机物的结构简式如图,下列关于该有机物的叙述正确的是( )
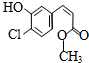

| A. | 该有机物的摩尔质量为200 | |
| B. | 该有机物属于芳香烃 | |
| C. | 该有机物可发生取代、加成、加聚、氧化、还原、消去反应 | |
| D. | 1 mol该有机物在适当条件下,最多可与4mol NaOH和4mol H2反应 |
7.在FeCl3和CuCl2的混合溶液中加入过量铁粉,反应完全后剩余固体的质量大于加入的铁粉质量.已知原混合溶液中FeCl3为0.4mol,则CuCl2的物质的量可能是( )
| A. | 0.2 mol | B. | 0.6 mol | C. | 1.2 mol | D. | 2 mol |
14.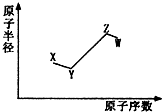 短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
 短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )| A. | X和Z、Y和W处于同一主族 | |
| B. | 4种元素形成的各种单质中,Z单质的沸点最高 | |
| C. | W单质与X、Y、Z的最简单氢化物都可以发生反应 | |
| D. | 元素氧化物所对应的水化物酸性:W>Z>X |
11.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 玻璃钢是钢与玻璃纤维形成的复合材料 | |
| B. | 氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| C. | 石油化工废弃物易造成水体富营养化 | |
| D. | 硫酸铵是常用的一种硝态氮肥 |
8.如图是部分短周期主族元素原子半径与原子序数的关系图.下列说法不正确的是( )


| A. | 离子半径:d3+<f- | |
| B. | 原子失电子能力:c>d | |
| C. | 最简单气态氢化物的热稳定性:a<e | |
| D. | b、c两元素可组成既含离子键又含共价键的化合物 |


 .
. .
. ,反应类型酯化反应.
,反应类型酯化反应. )
) .
.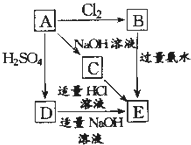 在如图式中,E是不溶于水的白色胶状物质,试推断:
在如图式中,E是不溶于水的白色胶状物质,试推断: