题目内容
18.已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )| A. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g);△H=+242kJ•mol-1 | B. | 2H2(g)+O2(g)+2H2O(l);△H=-484kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=+242kJ•mol-1 | D. | 2H2(g)+O2(g)=2H2O(g);△H=-484kJ•mol-1 |
分析 依据通过条件和热化学方程式的书写方法,标注物质聚集状态,对应量的焓变,配平写出.
解答 解:已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,则氢气燃烧的热化学方程式是:2H2(g)+O2(g)=2H2O(g);△H=-484kJ•mol-1.故选B.
点评 本题考查了热化学方程式的书写方法,物质聚集状态和焓变是解题的关键,题目较简单.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
9.下列化学用语表示正确的是( )
| A. | Mg2+的结构示意图: | |
| B. | 乙酸的化学式:CH3CH2OH | |
| C. | 硫酸钾的电离方程式:K2SO4═${K}_{2}^{+}$+${SO}_{4}^{2-}$ | |
| D. | N2的结构式:N≡N |
6.下列物质中,能够导电的电解质是( )
| A. | Cu丝 | B. | 熔融的MgCl2 | C. | 酒精 | D. | 蔗糖 |
13.化学平衡主要研究下列哪一类反应的规律( )
| A. | 可逆反应 | B. | 任何反应 | C. | 溶液间反应 | D. | 气体间反应 |
10.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O7 2-(橙色)+H2O?2H++2CrO42- (黄色),
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O7 2->Fe3+ | |
| C. | CrO42- 和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
7.下列各组物质中,所含电子数相同的是( )
| A. | 0.5mol37Cl2和16g O2 | B. | 5.6L N2(标准状况)和11g CO2 | ||
| C. | 20g D2O和10g H2 | D. | 224mL D2和0.1mol N2 |
11.化学科学需要借助化学专用语言来描述,下列有关化学用语正确( )
| A. | CO2的电子式为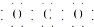 | B. | Cl-的结构示意图为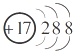 | ||
| C. | NaCl的电子式为Na+Cl- | D. | HCl的电子式为HCl |
 金属镁及其化合物在生活、工农业生产等方面有广泛的应用.
金属镁及其化合物在生活、工农业生产等方面有广泛的应用.