题目内容
3.(1)电解池就是把电能转化化学能的装置(2)常温下KW数值=1×10-14.
(3)常温下,某溶液中的c(H+)=5.0×10-7 mol•L-1,则此时c(OH-)=2.0×10-8mol•L-1.
分析 (1)电解池是将电能转化为化学能的装置;
(2)常温下水的离子积常数是一个定值,KW=1×10-14;
(3)根据Kw=c(H+)•c(OH-)来计算回答.
解答 解:(1)电解池是将电能转化为化学能的装置;故答案为:电能;化学能;
(2)常温下水的离子积常数是一个定值,KW=1×10-14;故答案为:1×10-14;
(3)常温下,水的离子积常Kw=c(H+)•c(OH-)=1×10-14;所以c(OH-)=$\frac{Kw}{c({H}^{+})}$=$\frac{1×1{0}^{-14}}{5.0×1{0}^{-7}}$=2.0×10-8,故答案为:2.0×10-8.
点评 本题涉及电解池的能量转化、水的离子及常数表达式以及计算等方面的知识,属于基本知识的考查,难度不大.

练习册系列答案
相关题目
13.表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
18.已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
| A. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g);△H=+242kJ•mol-1 | B. | 2H2(g)+O2(g)+2H2O(l);△H=-484kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=+242kJ•mol-1 | D. | 2H2(g)+O2(g)=2H2O(g);△H=-484kJ•mol-1 |
12.用Cu2O可制备环保防污涂料.有一种制备Cu2O的方法是向CuSO4溶液中加入Na2SO3,加热,保持微沸一段时间,过滤得到Cu2O固体.已知:Cu2O+2H+→Cu+Cu2++H2O.下列说法正确的是( )
| A. | 反应过程的离子方程式:2Cu2++3SO32-→Cu2O↓+SO42-+2SO2↑ | |
| B. | 反应过程的离子方程式:2Cu2++3SO32-+2H2O→Cu2O↓+SO42-+4H+ | |
| C. | 加入过量Na2SO3有利于控制溶液的pH | |
| D. | 在酸性条件下,若有14.4g Cu2O变质,转移电子0.02mol |
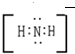
16.以下是四种不同分子,中心原子上存在2对孤电子对的是( )
| A. |  | B. |  | C. |  | D. | H2S |
 、
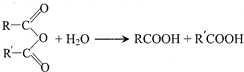
、 .
.
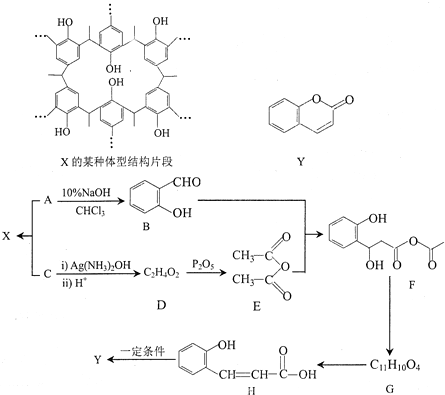
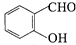 中的官能团名称为醛基、羟基
中的官能团名称为醛基、羟基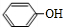 ,DCH3COOH,G
,DCH3COOH,G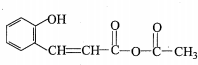

 )氮原子上的氢原子可以像A上的氢原子一样与C发生加成反应,再缩聚成高分子化合物.写出尿素与C在一定条件下生成线性高分子化合物的化学方程式
)氮原子上的氢原子可以像A上的氢原子一样与C发生加成反应,再缩聚成高分子化合物.写出尿素与C在一定条件下生成线性高分子化合物的化学方程式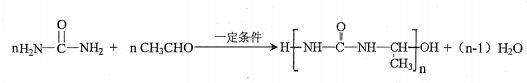
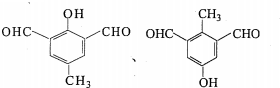 .
.