题目内容
下列关于1mol/L Na2SO4溶液的说法正确的是( )
| A、将142g Na2SO4溶于少量水后再稀释到 100mL |
| B、1 L溶液中含有142 g Na2SO4 |
| C、1 mol Na2SO4溶于1 L蒸馏水中 |
| D、溶液中含有1molNa+ |
考点:物质的量浓度的相关计算
专题:
分析:A.n(Na2SO4)=
=1mol,该溶液中硫酸钠的物质的量浓度=
;
B.n(Na2SO4)=
=1mol,该溶液中硫酸钠的物质的量浓度=
;
C.1 mol Na2SO4溶于1 L蒸馏水中,导致溶液体积大于1L;
D.溶液中含有1mol钠离子,但不能说明硫酸钠的物质的量浓度为1mol/L.
| 142g |
| 142g/mol |
| 1mol |
| 0.1L |
B.n(Na2SO4)=
| 142g |
| 142g/mol |
| 1mol |
| 1L |
C.1 mol Na2SO4溶于1 L蒸馏水中,导致溶液体积大于1L;
D.溶液中含有1mol钠离子,但不能说明硫酸钠的物质的量浓度为1mol/L.
解答:
解:A.n(Na2SO4)=
=1mol,该溶液中硫酸钠的物质的量浓度=
=10mol/L,故A错误;
B.n(Na2SO4)=
=1mol,该溶液中硫酸钠的物质的量浓度=
=1mol/L,故B正确;
C.1 mol Na2SO4溶于1 L蒸馏水中,导致溶液体积大于1L,导致溶液的物质的量浓度小于1mol/L,故C错误;
D.溶液中含有1mol钠离子,根据n=CV知,物质的量与物质的量浓度和溶液体积有关,溶液体积未知,所以不能说明硫酸钠的物质的量浓度为1mol/L,故D错误;
故选B.
| 142g |
| 142g/mol |
| 1mol |
| 0.1L |
B.n(Na2SO4)=
| 142g |
| 142g/mol |
| 1mol |
| 1L |
C.1 mol Na2SO4溶于1 L蒸馏水中,导致溶液体积大于1L,导致溶液的物质的量浓度小于1mol/L,故C错误;
D.溶液中含有1mol钠离子,根据n=CV知,物质的量与物质的量浓度和溶液体积有关,溶液体积未知,所以不能说明硫酸钠的物质的量浓度为1mol/L,故D错误;
故选B.
点评:本题考查物质的量浓度,侧重考查基本概念,明确物质的量浓度的含义是解本题关键,注意C=
中V指溶液体积不是溶剂体积,为易错点.
| n |
| V |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质能导电,且为电解质的是( )
| A、蔗糖 |
| B、KNO3晶体 |
| C、盐酸 |
| D、熔化的NaCl |
在密闭容器中进行如下反应:X2(g)+3Y2(g)?2Z(g),X2、Y2、Z的起始浓度分别为0.2mol?L-1、0.6mol?L-1、0.4mol?L-1,当平衡时下列数据肯定不正确的是( )
| A、X2为0.3 mol?L-1,Y2为0.9 mol?L-1 |
| B、Y2为1.0 mol?L-1 |
| C、X2为0.3 mol?L-1,Z为0.2 mol?L-1 |
| D、Z为1.0 mol?L-1 |
某氯化镁溶液的密度为1.6g?cm-3,其中镁离子的质量分数为5%,300mL该溶液中Cl-离子的物质的量约等于( )
| A、0.37 mol |
| B、0.63mol |
| C、2 mol |
| D、1.5mol |
某烃的结构简式为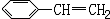 ,它不可能具有的性质是( )
,它不可能具有的性质是( )
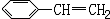 ,它不可能具有的性质是( )
,它不可能具有的性质是( )| A、它能发生加成反应 |
| B、它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
| C、它能发生取代反应 |
| D、它能发生加聚反应 |
已知:①2Fe3++Cu=2Fe2++Cu2+ ②2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O③Cl2+2Fe2+=2Cl-+2Fe3+,则下列关于微粒氧化性的判断正确的是( )
| A、Fe3+>Cu2+>MnO4->Cl2 |
| B、Cu2+>Fe3+>Cl2>MnO4- |
| C、MnO4->Cl2>Fe3+>Cu2+ |
| D、Cl2>MnO4->Cu2+>Fe3+ |
下列电离方程式不正确的是( )
| A、Al2 (SO4)3=2Al3++3SO42- |
| B、Ba(OH)2=Ba2++2OH- |
| C、Na2SO4=Na2++SO42- |
| D、NH4NO3=NH4++NO3- |
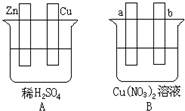 对如图中两极加以必要的连接并填空:
对如图中两极加以必要的连接并填空: