题目内容
某烃的结构简式为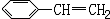 ,它不可能具有的性质是( )
,它不可能具有的性质是( )
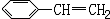 ,它不可能具有的性质是( )
,它不可能具有的性质是( )| A、它能发生加成反应 |
| B、它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
| C、它能发生取代反应 |
| D、它能发生加聚反应 |
考点:有机物的结构和性质
专题:
分析:由结构简式可知,分子中含苯环和双键,结合苯、烯烃的性质来解答.
解答:
解:A.含苯环和双键,能发生加成反应,故A正确;
B.含双键,则它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色,故B正确;
C.苯环上的H可发生取代反应,故C错误;
D.含双键,能发生加聚反应,故D正确;
故选C.
B.含双键,则它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色,故B正确;
C.苯环上的H可发生取代反应,故C错误;
D.含双键,能发生加聚反应,故D正确;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃性质的考查,题目难度不大.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
下列说法正确的是( )
| A、HR溶液的导电性较弱,所以HR属于弱酸 |
| B、某化合物溶于水导电,该化合物一定是电解质 |
| C、NaCl是电解质,食盐的水溶液也是电解质 |
| D、根据电解质在水溶液中的电离程度,将电解质分为强电解质和弱电解质 |
已知反应3Cu+8HNO3(稀)═Cu(NO3)2+2NO↑+4H2O.当生成2molNO时,下列说法正确的是( )
| A、有2molHNO3被还原 |
| B、转移的电子数目为6mol |
| C、有8molHNO3参加反应 |
| D、HNO3只作氧化剂 |
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是:2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、101kPa下△H=-113kJ?mol-1,△S=-145J?mol-1?K-1.下列说法中不正确的是( )
| A、该反应中反应物总能量高于生成物的总能量 |
| B、该反应只能在较高温度下才能自发进行 |
| C、汽车尾气中的这两种气体均会与人体血红蛋白结合而使人中毒 |
| D、该反应在较低温度下能自发进行,高温和催化剂条件只是加快反应的速率 |
下列关于1mol/L Na2SO4溶液的说法正确的是( )
| A、将142g Na2SO4溶于少量水后再稀释到 100mL |
| B、1 L溶液中含有142 g Na2SO4 |
| C、1 mol Na2SO4溶于1 L蒸馏水中 |
| D、溶液中含有1molNa+ |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| B、标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA |
| C、铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标况下) |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
下列离子方程式正确的是( )
| A、稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B、氧化镁与稀盐酸混合:MgO+2H+=Mg2++H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
当光束通过下列分散系:①稀硫酸 ②雾 ③蒸馏水 ④墨水,能观察到丁达尔效应的有( )
| A、①③ | B、②③ | C、②④ | D、③④ |