题目内容
在密闭容器中进行如下反应:X2(g)+3Y2(g)?2Z(g),X2、Y2、Z的起始浓度分别为0.2mol?L-1、0.6mol?L-1、0.4mol?L-1,当平衡时下列数据肯定不正确的是( )
| A、X2为0.3 mol?L-1,Y2为0.9 mol?L-1 |
| B、Y2为1.0 mol?L-1 |
| C、X2为0.3 mol?L-1,Z为0.2 mol?L-1 |
| D、Z为1.0 mol?L-1 |
考点:化学反应的可逆性
专题:
分析:化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答:
解:若反应向正反应进行到达平衡,X2、Y2的浓度最小,Z的浓度最大,假定完全反应,则:
根据方程式 X2(气)+3Y2(气)?2Z(气),
开始(mol/L):0.2 0.6 0.4
变化(mol/L):0.2 0.6 0.4
平衡(mol/L):0 0 0.8
若反应逆正反应进行到达平衡,X2、Y2的浓度最大,Z的浓度最小,假定完全反应,则:
根据方程式 X2(气)+3Y2(气)?2Z(气),
开始(mol/L):0.2 0.6 0.4
变化(mol/L):0.2 0.6 0.4
平衡(mol/L):0.4 1.2 0
由于为可能反应,物质不能完全转化所以平衡时浓度范围为0<c(X2)<0.4,0<c(Y2)<1.2,0<c(Z)<0.8.
故选D.
根据方程式 X2(气)+3Y2(气)?2Z(气),
开始(mol/L):0.2 0.6 0.4
变化(mol/L):0.2 0.6 0.4
平衡(mol/L):0 0 0.8
若反应逆正反应进行到达平衡,X2、Y2的浓度最大,Z的浓度最小,假定完全反应,则:
根据方程式 X2(气)+3Y2(气)?2Z(气),
开始(mol/L):0.2 0.6 0.4
变化(mol/L):0.2 0.6 0.4
平衡(mol/L):0.4 1.2 0
由于为可能反应,物质不能完全转化所以平衡时浓度范围为0<c(X2)<0.4,0<c(Y2)<1.2,0<c(Z)<0.8.
故选D.
点评:本题考查了化学平衡的建立,难度不大,关键是利用可逆反应的不完全性,运用极限假设法解答,假设法是解化学习题的常用方法.

练习册系列答案
相关题目
HA为酸性略强于醋酸的一元弱酸.在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)>c(OH-)>c(A-)>c(H+) |
| C、c(Na+)+c(H+)=c(A-)+c(OH-) |
| D、c(Na+)+c(OH-)=c(A-)+c(H+) |
已知反应3Cu+8HNO3(稀)═Cu(NO3)2+2NO↑+4H2O.当生成2molNO时,下列说法正确的是( )
| A、有2molHNO3被还原 |
| B、转移的电子数目为6mol |
| C、有8molHNO3参加反应 |
| D、HNO3只作氧化剂 |
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要的作用.下列关于实验的叙述中正确的有( )
| A、不慎碰翻燃着的酒精灯失火,应立即用湿布灭火 |
| B、不慎将酸沾到皮肤或衣物上,应立即用浓NaOH清洗 |
| C、用托盘天平称量物品质量时,物品应置于右盘 |
| D、实验时应节约药品,实验剩余的药品应放回原试剂瓶 |
| E、可燃性气体点燃前一定要验纯 |
| F、使用分液漏斗前须检查其是否漏水 |
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是:2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、101kPa下△H=-113kJ?mol-1,△S=-145J?mol-1?K-1.下列说法中不正确的是( )
| A、该反应中反应物总能量高于生成物的总能量 |
| B、该反应只能在较高温度下才能自发进行 |
| C、汽车尾气中的这两种气体均会与人体血红蛋白结合而使人中毒 |
| D、该反应在较低温度下能自发进行,高温和催化剂条件只是加快反应的速率 |
下列关于1mol/L Na2SO4溶液的说法正确的是( )
| A、将142g Na2SO4溶于少量水后再稀释到 100mL |
| B、1 L溶液中含有142 g Na2SO4 |
| C、1 mol Na2SO4溶于1 L蒸馏水中 |
| D、溶液中含有1molNa+ |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| B、标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA |
| C、铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标况下) |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
下列反应的离子方程式正确的是( )
| A、向含有Hg2+的废水中加入Na2S:Hg2++S2-═HgS |
| B、用碳酸氢钠作为抗酸药来中和胃酸 2H++CO32-═H2O+CO2↑ |
| C、用熟石灰来中和酸性废水 Ca(OH)2+2H+═Ca2++2H2O |
| D、用H2SO4来中和碱性废水 2H++2OH-═H2O |
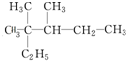
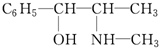 麻黄素中含氧官能团的名称是
麻黄素中含氧官能团的名称是