题目内容
下列电离方程式错误的是( )
| A、K2CO3═2K++CO32- |
| B、NaHSO4═H++SO42-+Na+ |
| C、KHCO3═K++H++CO32- |
| D、NH4Cl═NH4++Cl- |
考点:电离方程式的书写
专题:
分析:A.K2CO3属于强电解质,溶液中完全电离,碳酸根离子不能拆开,电离方程式用等号;
B.NaHSO4是强酸强碱酸式盐,属强电解质,溶液中完全电离,电离出Na+、H+、SO42-离子;
C.碳酸氢钾在溶液中电离出钾离子和碳酸氢根离子,碳酸氢根离子不能拆开,电离方程式用等号;
D.NH4Cl属于强电解质,溶液中完全电离,铵根离子不能拆开,电离方程式用等号.
B.NaHSO4是强酸强碱酸式盐,属强电解质,溶液中完全电离,电离出Na+、H+、SO42-离子;
C.碳酸氢钾在溶液中电离出钾离子和碳酸氢根离子,碳酸氢根离子不能拆开,电离方程式用等号;
D.NH4Cl属于强电解质,溶液中完全电离,铵根离子不能拆开,电离方程式用等号.
解答:
解:A.K2CO3为强电解质,在溶液中完全电离,生成K+和CO32-离子,电离方程式为K2CO3=2K++CO32-,故A正确;
B.硫酸氢钠属于二元强酸硫酸的酸式盐,能完全电离:NaHSO4=Na++H++SO42-,故B正确;
C.碳酸氢钾属于强电解质,溶液中完全电离,碳酸氢根离子不能拆开,其正确的电离方程式为:KHCO3═K++HCO3-,故C错误;
D.NH4Cl为强电解质,在溶液中完全电离,生成NH4+和Cl-,电离方程式为NH4Cl═NH4++Cl-,故D正确;
故选C.
B.硫酸氢钠属于二元强酸硫酸的酸式盐,能完全电离:NaHSO4=Na++H++SO42-,故B正确;
C.碳酸氢钾属于强电解质,溶液中完全电离,碳酸氢根离子不能拆开,其正确的电离方程式为:KHCO3═K++HCO3-,故C错误;
D.NH4Cl为强电解质,在溶液中完全电离,生成NH4+和Cl-,电离方程式为NH4Cl═NH4++Cl-,故D正确;
故选C.
点评:本题考查了电离方程式的书写判断,题目难度不大,注意掌握强电解质、弱电解质的判断方法,明确电离方程式的书写原则为解答关键,试题培养了学生规范答题的能力.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
下列各表述与示意图一致的是( )


| A、图①表示N2O4(g)?2NO2(g)△H>0,N2O4转化率随温度、时间的变化 |
| B、图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
| C、图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化 |
| D、图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
下列说法中正确的是( )
| A、1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L |
| B、从1L2mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1mol/L |
| C、配制480mL0.5 mol/L的CuSO4溶液,需62.5g胆矾 |
| D、10g98%的硫酸(密度为1.84 g?cm-3)与10 mL18.4 mol?L-1的硫酸的浓度不同 |
某溶液中大量存在以下浓度的离子:0.2mol/LCl-、0.4mol/LSO42-、0.1mol/LAl3+、0.3mol/LH+、M,则M及其物质的量浓度可能为( )
| A、Na+0.2mol/L |
| B、Zn2+0.2mol/L |
| C、CO32- 0.2mol/L |
| D、Ca2+0.1mol/L |
质量为1g的H2O中含m个氢原子,则阿伏加德罗常数为( )
A、
| ||
| B、9m | ||
| C、2m | ||
| D、m |
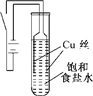 某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
某化学研究小组以铜为电极电解饱和食盐水,探究过程如下: