题目内容
某同学称取20g碳酸钠和碳酸氢钠的混合物,将混合物充分加热后得到气体1.68L(标准状况)
(1)混合物中碳酸氢钠的质量分数.
(2)用加热后的残留物配制成250ml溶液,则所得溶液的物质的量浓度是多少?(结果保留到小数点后两位)
(1)混合物中碳酸氢钠的质量分数.
(2)用加热后的残留物配制成250ml溶液,则所得溶液的物质的量浓度是多少?(结果保留到小数点后两位)
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:(1)加热发生反应:2NaHCO3
Na2CO3+H2O+CO2↑,根据n=
计算二氧化碳的物质的量,根据方程式计算碳酸氢钠物质的量,再根据m=nM计算碳酸氢钠的质量,进而计算原混合物中碳酸氢钠的质量分数;
(2)计算原混合物中碳酸钠的质量,加热后的最终残留物为碳酸钠,根据钠离子守恒计算最终碳酸钠的物质的量,再根据c=
计算所得碳酸钠溶液物质的量浓度.
| ||
| V |
| Vm |
(2)计算原混合物中碳酸钠的质量,加热后的最终残留物为碳酸钠,根据钠离子守恒计算最终碳酸钠的物质的量,再根据c=
| n |
| V |
解答:
解:(2)得到气体1.68L(标准状况)为二氧化碳,其物质的量=
=0.075mol,
2NaHCO3
Na2CO3+H2O+CO2↑
2 1
n(NaHCO3) 0.075mol
则n(NaHCO3)=
=0.15mol
故m(NaHCO3)=0.15mol×84g/mol=12.6g
故碳酸氢钠的质量分数=
×100%=63%,
答:混合物中碳酸氢钠的质量分数为63%;
(2)原混合物中碳酸钠的质量为:20g-12.6g=7.4g,加热后的最终残留物为碳酸钠,根据钠离子守恒计算最终碳酸钠的物质的量为0.15mol×
+
=0.1448mol,故碳酸钠溶液物质的量浓度为
=0.58mol/L,
答:所得溶液的物质的量浓度是0.58mol/L.
| 1.68L |
| 22.4L/mol |
2NaHCO3
| ||
2 1
n(NaHCO3) 0.075mol
则n(NaHCO3)=
| 0.075×2 |
| 1 |
故m(NaHCO3)=0.15mol×84g/mol=12.6g
故碳酸氢钠的质量分数=
| 12.6g |
| 20g |
答:混合物中碳酸氢钠的质量分数为63%;
(2)原混合物中碳酸钠的质量为:20g-12.6g=7.4g,加热后的最终残留物为碳酸钠,根据钠离子守恒计算最终碳酸钠的物质的量为0.15mol×
| 1 |
| 2 |
| 7.4g |
| 106g/mol |
| 0.1448mol |
| 0.25L |
答:所得溶液的物质的量浓度是0.58mol/L.
点评:本题考查化学方程式有关计算,难度不大,侧重对基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如图:MFe2Ox
MFe2Oy,则下列判断正确的是( )
| 常温下 |
| SO2 |
| A、MFe2Ox是氧化剂 |
| B、x<y |
| C、SO2是该反应的催化剂 |
| D、SO2发生氧化反应且氧化性:MFe2Oy>SO2 |
某物质熔融状态可导电,固态可导电,将其投入水中溶液也可导电,推测该物质可能是( )
| A、金属 | B、非金属 |
| C、可溶性碱 | D、可溶性盐 |
下列电离方程式错误的是( )
| A、K2CO3═2K++CO32- |
| B、NaHSO4═H++SO42-+Na+ |
| C、KHCO3═K++H++CO32- |
| D、NH4Cl═NH4++Cl- |
下列各电离方程式中书写正确的是( )
| A、HClO═H++ClO- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、Al(OH)3?Al3++3OH- |
| D、NaH2PO4?Na++H2PO4- |
下列离子方程式书写正确的是( )
| A、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O |
| B、硫酸溶液与氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
| D、FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ |
能正确表示下列反应的离子方程式是( )
| A、硫酸铝溶液中加入过量氨水Al3++3OH-═Al(OH)3↓ | ||||
| B、向水中通入氯气:Cl2+H2O=2H++Cl-+ClO- | ||||
C、MnO2与浓盐酸共热制Cl2:MnO2+4H++2Cl-
| ||||
| D、向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O |
下列说法错误的是( )
A、用数轴表示分散系的分类: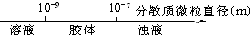 |
| B、已知氯酸钾与蔗糖(C12H22O11)反应的产物为KCl、CO2和水,则氧化产物与还原产物的物质的量之比为2:3 |
| C、10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49% |
| D、可以用Ba(OH)2和焰色反应鉴别NaHCO3、NaCl、KCl、K2SO4 |
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺的状况 |
| B、大量使用化肥和农药,以提高农作物产量 |
| C、含磷化合物的排放是“水华”和“赤潮”产生的原因 |
| D、安装煤炭“固硫”装置,降低酸雨发生率 |