题目内容
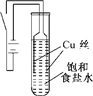 某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:实验1:如右图所示连接装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10.随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色.
实验2:将实验1中试管底部的橙黄色沉淀取出,分装在两支小试管中,以后的操作和现象如下:
| 序号 | 操作 | 现象 |
| ① | 滴入稀硝酸溶液 | 沉淀溶解,有无色气泡产生,最终得到蓝色溶液 |
| ② | 滴入稀硫酸溶液 | 橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
| 物质 | 颜色 | 物质 | 颜色 |
| 氯化铜 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 氢氧化亚铜(不稳定) | 橙黄色 |
| 碱式氯化铜 | 绿色 | 氢氧化铜 | 蓝色 |
| 氧化亚铜 | 砖红色或橙黄色 | 氯化亚铜 | 白色 |
(1)铜的常见正化合价为
(2)阴极上发生的反应为
(3)写出实验2中①、②的离子方程式:
①
考点:电解原理
专题:电化学专题
分析:(1)根据氯化铜、氧化亚铜判断铜的化合价;根据固体颜色判断试管底部橙黄色沉淀的物质成分;
(2)根据放电顺序及实验现象判断生成物,并写出电极反应式;
(3)根据实验现象确定生成物并写出相应的离子方程式;
(2)根据放电顺序及实验现象判断生成物,并写出电极反应式;
(3)根据实验现象确定生成物并写出相应的离子方程式;
解答:
解析:(1)铜有+1价和+2价,据实验1的现象说明橙黄色沉淀较稳定,再结合铜的化合物的颜色知该物质应为Cu2O,而Cu2O也符合实验2中的要求,故答案为:+1、+2;Cu2O;
(2)在阴极上H+放电,反应为2H++2e-═H2↑,而阳极为铜,电极本身失电子,铜失电子生成亚铜离子进入溶液,亚铜离子和氯离子生成氯化亚铜白色沉淀即反应为Cu-e-+Cl-═CuCl↓,故答案为:2H++2e-═H2↑Cu+Cl--e-═CuCl↓;
(3)根据实验现象及硝酸和氧化亚铜的性质、及常见铜的化合物颜色判断,生成物是一氧化氮、硝酸铜和水,所以离子方程式为3Cu2O+2H++2NO3-=6Cu2++2NO↑+7H2O
②根据实验现象及常见铜的化合物颜色,生成物是铜、硫酸铜和水,所以离子方程式为Cu2O+2H+=Cu+Cu2++H2O.
故答案为:3Cu2O+2H++2NO3-=6Cu2++2NO↑+7H2O;Cu2O+2H+=Cu+Cu2++H2O.
(2)在阴极上H+放电,反应为2H++2e-═H2↑,而阳极为铜,电极本身失电子,铜失电子生成亚铜离子进入溶液,亚铜离子和氯离子生成氯化亚铜白色沉淀即反应为Cu-e-+Cl-═CuCl↓,故答案为:2H++2e-═H2↑Cu+Cl--e-═CuCl↓;
(3)根据实验现象及硝酸和氧化亚铜的性质、及常见铜的化合物颜色判断,生成物是一氧化氮、硝酸铜和水,所以离子方程式为3Cu2O+2H++2NO3-=6Cu2++2NO↑+7H2O
②根据实验现象及常见铜的化合物颜色,生成物是铜、硫酸铜和水,所以离子方程式为Cu2O+2H+=Cu+Cu2++H2O.
故答案为:3Cu2O+2H++2NO3-=6Cu2++2NO↑+7H2O;Cu2O+2H+=Cu+Cu2++H2O.
点评:本题以电解原理为载体考查了铜的常见化合物的性质及颜色,本题只有结合铜的常见化合物颜色才能正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列电离方程式错误的是( )
| A、K2CO3═2K++CO32- |
| B、NaHSO4═H++SO42-+Na+ |
| C、KHCO3═K++H++CO32- |
| D、NH4Cl═NH4++Cl- |
下列说法错误的是( )
A、用数轴表示分散系的分类: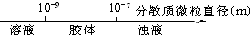 |
| B、已知氯酸钾与蔗糖(C12H22O11)反应的产物为KCl、CO2和水,则氧化产物与还原产物的物质的量之比为2:3 |
| C、10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49% |
| D、可以用Ba(OH)2和焰色反应鉴别NaHCO3、NaCl、KCl、K2SO4 |
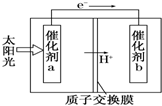 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A、催化剂b表面的反应是CO2+2H++2e-═HCOOH |
| B、催化剂a表面发生氧化反应,有O2产生 |
| C、催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D、该过程是将太阳能转化为化学能的过程 |
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺的状况 |
| B、大量使用化肥和农药,以提高农作物产量 |
| C、含磷化合物的排放是“水华”和“赤潮”产生的原因 |
| D、安装煤炭“固硫”装置,降低酸雨发生率 |
一定温度下存在反应:2SO2(g)+O2(g)?2SO3(g),其正反应放热.现有两个体积相同的密闭容器Ⅰ、Ⅱ,中间隔板不漏气且可自由滑动,按如图所示投料.达到平衡时,下列说法正确的是( )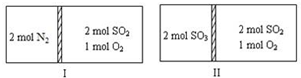

| A、容器Ⅰ、Ⅱ的右室中SO3的体积分数相同 |
| B、容器Ⅰ、Ⅱ的右室中反应速率I<II |
| C、平衡时容器Ⅰ、Ⅱ中的隔板均应在中间 |
| D、容器II若为绝热容器(隔板不导热),则容器II右室中SO2的转化率与左室SO3的转化率之和小于1 |
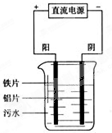 电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图.
电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图.