题目内容
10.对于可逆反应,A2(g)+3B2(g)?2AB3(g)(正反应吸热),下列图象正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 对应可逆反应A2(g)+3B2(g)?2AB3(g),△H>0,升高温度,反应速率加快,缩短到达平衡的时间,平衡向正反应方向移动,正反应速率增大的更多,反应物的含量减少;正反应为体积减小的反应,增大压强,平衡正向移动,反应物的含量减小,以此来解答.
解答 解:A.升高温度,向正反应方向移动,正反应速率大于逆反应速率,图象与实际相符,故A正确;
B.升高温度,反应速率加快,到达平衡的时间缩短,平衡向正反应方向移动,产物的含量升高,图象与实际不相符,故B错误;
C.增大压强,平衡正向移动,产物的含量增大,图象与实际不相符,故C错误;
D.但升高温度,平衡向正反应方向移动,反应物的含量减少,图象与实际不相符合,故D错误;
故选A.
点评 本题考查化学平衡移动图象问题,难度中等,注意根据化学方程式的特点分析温度、压强对化学平衡移动的影响,注意D选项中采取“定一议二”原则进行分析.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
20. 一定温度下,将1mol A和1mol B气体充入2L密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1mol A和1mol B气体充入2L密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
 一定温度下,将1mol A和1mol B气体充入2L密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1mol A和1mol B气体充入2L密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A. | 该反应方程式中的x=l | |
| B. | 0~t1时,用A表示的反应速率υ(A)=0.50mol/(L•min) | |
| C. | t2和t3时,改变的条件分别是加入催化剂和移去少量物质D | |
| D. | t1~t3间,该反应的平衡常数均为4 |
1.某温度下,对可逆反应:2X(g)+Y(g)?Z(g)+W(s)△H>0的下列叙述不正确的是( )
| A. | 容器体积不变,充入与反应体系不反应的N2,反应速率不变;压强不变,充入N2,反应速率减小 | |
| B. | 升高温度时,正反应速率增大,逆反应速率也一定增大 | |
| C. | 恒温恒容下,若X、Y起始物质的量之比为2:1,则X、Y的转化率始终相等 | |
| D. | 恒温恒压下,该反应达到平衡后若只增加Z的量,重新达到平衡,各物质的物质的量之比可能不变 |
18.在某温度下,可逆反应mA+nB?pC+qD的平衡常数为K,下列说法正确的是( )
| A. | K越大,达到平衡时,反应进行的程度越大 | |
| B. | K越小,达到平衡时,反应物的转化率越大 | |
| C. | K随反应物浓度的改变而改变 | |
| D. | K随温度和压强的改变而改变 |
5.羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)?COS(g)+H2(g) K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol.下列说法不正确的是( )
| A. | 降低温度,H2S浓度减小,表明该反应是放热反应 | |
| B. | 通入CO后,逆反应速率逐渐增大,直至再次平衡 | |
| C. | 反应前H2S物质的量为6mol | |
| D. | CO的平衡转化率为20% |
15.将35.0g锌粉与少量浓硫酸在加热的条件充分反应,共收集到混合气体11.2L(标准状况),则过量的锌粉的质量为( )
| A. | 1.0g | B. | 2.0g | C. | 2.5g | D. | 3.5g |
2.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
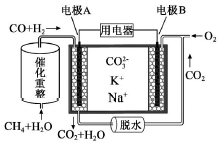

| A. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 反应CH4+H2O $\frac{\underline{催化剂}}{△}$ 3H2+CO,每消耗1molCH4转移12mol 电子 |
19.现有0.1mol•L-1醋酸溶液10mL,加蒸馏水稀释到1L后,下列变化中正确的是( )
①电离程度增大 ②c(CH3COOH)增大 ③CH3COO-数目增多 ④c(H+)增大
⑤导电性增强 ⑥$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大 ⑦c(OH-)增大.
①电离程度增大 ②c(CH3COOH)增大 ③CH3COO-数目增多 ④c(H+)增大
⑤导电性增强 ⑥$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大 ⑦c(OH-)增大.
| A. | ①②③⑦ | B. | ①③⑤⑥ | C. | ①③⑥⑦ | D. | ②④⑤⑥ |
20.通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一.下列反应的推断或解释正确的是( )
| 操作 | 可能的实验现象 | 解释 | |
| A | 某溶液中加入盐酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| B | 将SO2中通入硝酸钡溶液中 | 有白色沉淀生成 | BaSO3不溶于硝酸 |
| C | 同温同压下,用pH试纸测定相同浓度的碳酸钠和硫酸钠溶液的酸碱性 | 碳酸钠溶液显碱性,硫酸钠溶液显中性 | 碳酸钠发生了水解 |
| D | 向淀粉KI溶液中通入Cl2 | 溶液先变蓝后褪色 | Cl2先表现氧化性、后表现强氧化性 |
| A. | A | B. | B | C. | C | D. | D |