题目内容
9.下列各反应达到平衡后,减小压强或升高温度都能使化学平衡向正反应方向移动的是( )| A. | N2(g)+3H2(g)?2NH3(g) (正反应为放热反应) | |
| B. | C(s)+CO2(g)?2CO(g) (正反应为吸热反应) | |
| C. | 2NO2(g)?N2O4(g) (正反应为放热反应) | |
| D. | 3O2(g)?2O3(g) (正反应为吸热反应) |
分析 依据化学平衡移动原理可知,改变一个条件,平衡向减弱这种改变的方向进行,减小压强或升高温度都能使化学平衡向正反应方向移动,即正反应是气体体积增大的吸热反应,据此分析反应特征选择;
解答 解:A.正反应是放热反应,升温平衡逆向进行,故A错误;
B.正反应是气体体积增大的吸热反应,减小压强或升高温度都能使化学平衡向正反应方向移动,故B正确;
C.正反应是放热反应,升温平衡逆向进行,故C错误;
D.正反应是气体体积减小的吸热反应,减小压强平衡逆向进行,故D错误;
故选B.
点评 本题考查了影响化学平衡的因素分析判断,主要是反应特征和平衡移动原理的理解应用,题目较简单.

练习册系列答案
相关题目
19.下列实验操作中正确的是( )
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 鉴别己烯和苯:分别向己烯和苯中滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| C. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| D. | 检验卤代烃中的卤素原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色 |
20.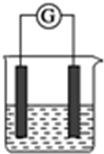 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )
 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
17.下列物质属于纯净物的是( )
| A. | 漂粉精 | B. | 铝热剂 | C. | 汽油 | D. | 纯碱 |
4.为达到表所列的实验目的,所采用的实验方法正确的是( )
| 实验目的 | 实验方法 | |
| A | 检验某混合溶液中是否有Cl- | 取样滴加AgNO3溶液 |
| B | 除去食盐中的少量氯化铵 | 加热 |
| C | 鉴别CO2和SO2 | 分别通入澄清石灰水 |
| D | 证明某地雨水样品呈酸性 | 取样滴入酚酞 |
| A. | A | B. | B | C. | C | D. | D |
14.证明淀粉在酶作用下只部分发生了水解的实验试剂是( )
| A. | 碘水 | B. | 碘水、烧碱溶液、新制的Cu(OH)2 | ||
| C. | 氢氧化钠溶液、银氨溶液 | D. | 烧碱溶液、新制的Cu(OH)2 |
18.能与Fe3+反应,且能证明Fe3+具有氧化性的是( )
①SCN- ②F ③Fe2+④Cu ⑤Zn ⑥OH-.
①SCN- ②F ③Fe2+④Cu ⑤Zn ⑥OH-.
| A. | ①②③ | B. | ②④⑤ | C. | ①③⑥ | D. | ①②⑤ |
19.某矿石由前20号元素中的四种组成,其化学式为WYZX4.X、Y、Z、W分布在三个周期,且原子序数依次增大,Y、Z处于相邻主族,Y、W为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等.则下列判断正确的是( )
| A. | 原子半径:W>Y>Z>X | |
| B. | 气态氢化物的稳定性:X>Z | |
| C. | Y、Z的氧化物都有两性 | |
| D. | 最高价氧化物对应水化物的碱性:Y>W |