��Ŀ����
2�����Ƽ���ҽ���ϳ�������������ۣ���һ�ֺϳ�·����ͼ��
��֪�������ͻ������백��NH3����R-NH2����Ӧ�������µİ������
�磺R1-CH=CH2+R2-NH2 $\stackrel{һ������}{��}$ R1-CH2-CH2-NH-R2
��
 +R3
+R3 $\stackrel{C_{2}H_{5}ONa}{��}$
$\stackrel{C_{2}H_{5}ONa}{��}$ +R2OH
+R2OH��1��B�к��������ŵ�����Ϊ������
��2����Ӧ�ٵķ�Ӧ����Ϊ�ӳɷ�Ӧ����Ӧ�ڵķ�Ӧ����ΪŨ���ᡢ���ȣ�
��3����Ӧ�۵Ļ�ѧ����ʽΪ
 ��
����4��C�Ľṹ��ʽΪ
 ��
����5������˵����ȷ����a������ĸ����
a����Ӧ��Ϊȡ����Ӧ
b�����Ƽ��뻯����G��Ϊͬϵ��
c��1mol D�������2mol NaOH������Ӧ
��6����֪A��NaOH��Һ��ˮ�����֮һ��һ�������ܸ߷��Ӳ��ϣ�PAANa���ĵ��壬д������PAANa�Ļ�ѧ����ʽ
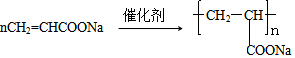 ��
����7����֪��CH2=CHCH3+Cl2 $\stackrel{500��}{��}$ CH2=CHCH2Cl+HCl���Ա�ϩ���Ҵ�Ϊ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ�A��д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ������
 ��
��
���� ��B�Ľṹ��ʽ��֪AΪCH2=CHCOOCH2CH3�������Ƽ��֪HΪ ���Ա�E��G�ķ���ʽ��֪EΪ
���Ա�E��G�ķ���ʽ��֪EΪ ����CΪ
����CΪ ��DΪ
��DΪ ����϶�Ӧ�л���Ľṹ�����ŵ����ʽ��1������6����
����϶�Ӧ�л���Ľṹ�����ŵ����ʽ��1������6����
��7���Ա�ϩ���Ҵ�Ϊ��ʼԭ�ϣ��ϳ�CH2=CHCOOCH2CH3��Ӧ������CH2=CHCOOH�����ɱ�ϩ����������ȡ����Ӧ����CH2=CHCH2OH��Ȼ��������ֱ�����CH2=CHCHO��CH2=CHCOOH�����Ҵ�����������Ӧ������CH2=CHCOOCH2CH3��
��� �⣺��1���ɽṹ��ʽ��֪B�к��������ŵ�����Ϊ�������ʴ�Ϊ��������
��2����Ӧ����A��C=C������C-C����Ϊ�ӳɷ�Ӧ����Ӧ��Ϊ������ȥ��Ӧ����Ӧ����ΪŨ���ᡢ���ȣ��ʴ�Ϊ���ӳɷ�Ӧ��Ũ���ᡢ���ȣ�
��3����Ӧ��Ϊ������Ӧ������ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4�������Ϸ�����֪CΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��a����Ӧ���м�ȡ��Hԭ�ӣ�Ϊȡ����Ӧ����a��ȷ��
b�����Ƽ��뻯����G���еĹ����Ų�ͬ�����߲���ͬϵ���b����
c��Dֻ������������������Һ��Ӧ����1mol D�������1mol NaOH������Ӧ����c����
�ʴ�Ϊ��a��
��6��AΪCH2=CHCOOCH2CH3��A��NaOH��Һ��ˮ������CH2=CHCOONa������̼̼˫�����ɷ����Ӿ۷�Ӧ������ʽΪ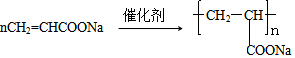 ��
��
�ʴ�Ϊ��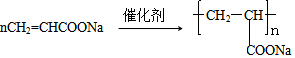 ��
��
��7���Ա�ϩ���Ҵ�Ϊ��ʼԭ�ϣ��ϳ�CH2=CHCOOCH2CH3��Ӧ������CH2=CHCOOH�����ɱ�ϩ����������ȡ����Ӧ����CH2=CHCH2OH��Ȼ��������ֱ�����CH2=CHCHO��CH2=CHCOOH�����Ҵ�����������Ӧ������CH2=CHCOOCH2CH3����Ӧ������Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л��ϳɣ�Ϊ�߿��������ͣ����ؿ���ѧ���ķ�����������Ŀ�Ѷ��еȣ��Ӻϳ�������ϳ����л�������ʿ��Խ������ʵ��ƶϣ��������ճ����л���ṹ������Ϊ���ؼ���

2SO2��g��+O2$?_{����}^{����}$2SO3��g��+QkJ����������������ǣ�������
| A�� | ����ѹǿ���÷�Ӧ�����淴Ӧ���ʿ��ܲ��� | |
| B�� | �����¶ȣ�����Ӧ���ʱ��淴Ӧ���ʼ�С�ij̶�С | |
| C�� | ��������������������ƽ�������ƶ���ƽ�ⳣ��Kֵ���� | |
| D�� | ����������ʵ�������0.5 molʱ�ﵽƽ�⣬��������·�Ӧ�ų�0.5 Q KJ������ |
| A�� | c��NH4+����c��NO3-����c��H+����c��OH-�� | B�� | c��NO3-����c��NH4+����c��H+����c��OH-�� | ||
| C�� | c��H+����c��NH4+����c��NO3-����c��OH-�� | D�� | c��OH-����c��NO3-����c��NH4+����c��H+�� |
| A�� | Ħ��������� | B�� | �����ܶ���� | C�� | ����������� | D�� | ������������� |
��1
| �� | X |
| Y | Z |
| ���ݱ�� | ����NaOH��Һ�����/mL | ��ҺpH | |
| HX | HZ | ||
| �� | 0 | 3 | 1 |
| �� | 20.00 | a | 7 |
| A�� | ������a��7 | |
| B�� | HX��HZ�������Ϻ�pH=1+lg2 | |
| C�� | Y��Z��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�߷ֽ��¶ȸ� | |
| D�� | 0��l000 mol/L Na2Y��ˮ��Һ�У�c��Y2-��+c��HY-��+c��H2Y��=0.1000 mol/L |
| ̼ | �� | Y | |
| X | �� | Z |
��1��ZԪ�������ڱ��е�λ��Ϊ�������ڢ�A�壮
��2������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�Si��
��3��������ʵ��˵��YԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����ac������ţ���
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1mol��õ��Ӷ�
c��Y������Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��4������һ������ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ�������������ϱ�������Ԫ����ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L2.2mol•L-1 NaOH��Һ��1molO2������������ķ���ʽ�����ʵ����ֱ�ΪNO��0.9mol��NO2��1.3mol����������ͭ���ʵ���Ϊ2mol��
| A�� | Ư����Һ�ڿ�����ʧЧ��ClO-+CO2+H2O�THClO+HCO3- | |
| B�� | ������Һ�еμӹ��������Ag��NH3��2++2H+�TAg++2NH4+ | |
| C�� | ������������ϡ���ᷴӦ��3Fe+2NO3-+8H+�T3Fe2++2NO��+4H2O | |
| D�� | ��ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3�T2FeO42-+3Cl-+H2O+4H+ |
| A�� | KC1 | B�� | SiO2 | C�� | SO3 | D�� | NaOH |
| A�� | 1.8 g D2O����NA������ | |
| B�� | ��״���£�22.4 L�����й��ۼ���ĿΪ19NA | |
| C�� | 5.35 g NH4Cl�����к���N-H���ĸ���Ϊ0.4NA | |
| D�� | �����½�0.1 mol FeͶ��������Ũ�����У�ת�Ƶĵ�����Ϊ0.3NA |