题目内容
10.如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )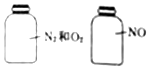
| A. | 摩尔质量相等 | B. | 气体密度相等 | C. | 气体质量相等 | D. | 所含分子数相等 |
分析 同温同压下,气体摩尔体积相等,体积相等的不同气体其物质的量相等,结合ρ=$\frac{M}{{V}_{m}}$、n=$\frac{V}{{V}_{m}}$解答.
解答 解:A.两个容器中物质的量相等,但其质量不一定相等,其平均摩尔质量不一定相等,故A错误;
B.根据ρ=$\frac{M}{{V}_{m}}$知,相同条件下,气体密度与摩尔质量成正比,两个容器中气体平均摩尔质量不一定相等,所以其密度不一定相等,故B错误;
C.左瓶中氮气与氧气的物质的量之比为不一定为1:1,故质量不一定相等,故C错误;
D.相同条件下气体的气体摩尔体积相等,则物质的量相等,由N=nNA可知分子数相等,故D正确.
故选D.
点评 本题考查阿伏伽德罗定律及其推论,为高频考点,侧重考查学生的分析能力和计算能力,明确物质的量公式中各个物理量之间的关系是解本题关键,熟练掌握物质的量有关公式,题目难度不大.

练习册系列答案
相关题目
15.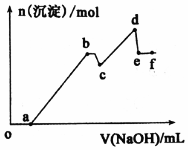 已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )
已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )
 已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )
已知25℃时,Ksp[Mg(OH)2]=5.61×l0-12,Ksp[Al(OH)3]=1.3×l0-33,Al(OH)3?AlO2-+H++H2O Ka=6.31×l0-13.某溶液中可能含有 H+、Na+、Mg2+、Al3+、Cl-、HCO3-等离子.向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关说法正确的是( )| A. | b 点沉淀-Al(OH)3;d 点沉淀-A1(OH)3和Mg(OH)2;e点溶质-NaA1O2 | |
| B. | 依据题意,用NaOH不能完全分离Mg2+和Al3+离子 | |
| C. | cd 段发生的反应为:Mg2++2OH-=Mg(OH)2↓ | |
| D. | bc 段发生的反应为:Al(OH)3+OH-=A1O2-+2H2O |
12.下列实验现象的描述中不正确的是( )
| A. | 铁丝在空气中燃烧,火星四射,产生红棕色的烟 | |
| B. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 在试管中加热铜绿有黑色固体生成 | |
| D. | 人造丝在酒精灯的火焰上灼烧会产生烧焦羽毛的气味 |
15.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法不正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 012 | 011 | 010 | 010 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-5 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数:K=1.44 | |
| D. | 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32mol气体Y,到达平衡时,n(Z)=0.024mol |
19.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 将气体X分别通入溴水和酸性高锰酸钾溶液中,两溶液均褪色 | 气体X一定是C2H4 |
| B | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32--强 |
| C | 向某溶液中先滴加少量氯水,再滴加2滴KSCN溶液,溶液变成血红色 | 原溶液中一定含有Fe2+ |
| D | 将H2S气体通入浓度均为0.01mol•L-l的ZnSO4和CuSO4混合溶液中,先出现CuS黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A. | A | B. | B | C. | C | D. | D |
7.可逆反应N2(g)+3H2(g)?2NH3(g)在密闭容器中进行,一段时间后测得c(N2)=1.5mol/L,c(H2)=0.6mol/L,c(NH3)=1.5mol/L,则此反应达到平衡后,下列数据可能正确的是( )
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
 已知A是一种黄绿色气体,由此推断:
已知A是一种黄绿色气体,由此推断:
 +R3
+R3 $\stackrel{C_{2}H_{5}ONa}{→}$
$\stackrel{C_{2}H_{5}ONa}{→}$ +R2OH
+R2OH .
. .
. .
. .
.