题目内容
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1.8 g D2O含有NA个中子 | |
| B. | 标准状况下,22.4 L己烷中共价键数目为19NA | |
| C. | 5.35 g NH4Cl固体中含有N-H键的个数为0.4NA | |
| D. | 常温下将0.1 mol Fe投入足量的浓硝酸中,转移的电子数为0.3NA |
分析 A、n=$\frac{m}{M}$ 计算物质的量,结合质子数+中子数=质量数计算中子数;
B、标况下,己烷为液态;
C、根据n=$\frac{m}{M}$ 计算出氯化铵的物质的量,氯化铵中含有4个氮氢键;
D、常温下铁在浓硝酸中发生钝化.
解答 解:A、1.8gD2O的物质的量为$\frac{1.8g}{20g/mol}$=0.09mol,而1mol重水中含10个中子,故0.09mol重水中含0.9NA个,故A错误;
B、标况下,己烷为液态,故B错误;
C、5.35g氯化铵的物质的量为$\frac{5.35g}{53.5g/mol}$=0.1mol,0.1mol氯化铵中含有0.4mol氮氢键,含有的N-H键个数为0.4NA,故C正确;
D、常温下铁在浓硝酸中发生钝化,不能继续反应,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用,气体摩尔体积条件分析应用,注意常温下铁在浓硝酸中发生钝化,题目难度中等.

练习册系列答案
相关题目
3.下列各图与表述一致的是( )
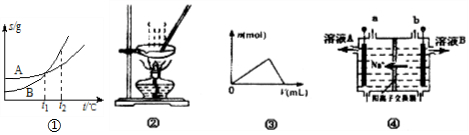

| A. | 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| B. | 用图②所示装置蒸发FeCl3溶液制备无水FeCl3 | |
| C. | 图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化 | |
| D. | 图④电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B |
7.可逆反应N2(g)+3H2(g)?2NH3(g)在密闭容器中进行,一段时间后测得c(N2)=1.5mol/L,c(H2)=0.6mol/L,c(NH3)=1.5mol/L,则此反应达到平衡后,下列数据可能正确的是( )
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
14.日常所用干电池其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2氧化吸收H2),电极反应可简化为:Zn-2e-═Zn2+、2NH4++2e-═2NH3+H2(NH3再用于结合Zn2+)根据上述叙述判断下列说法中正确的是( )
| A. | 干电池中Zn为正极,碳为负极 | |
| B. | 干电池可以实现化学能向电能的转化和电能向化学能的转化 | |
| C. | 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 | |
| D. | 干电池工作时,电子由碳极经外电路流向Zn极 |
4.FeCl2是一种常用的还原剂.有关数据如下:
查阅资料知:氯化铁遇水剧烈水解.实验室可以用如下方法来制备无水FeCl2.
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
11.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA | |
| B. | 12 g石墨烯(单层石墨)中含有六元环的个数为0.5NA | |
| C. | 0.1molFe与稀硝酸恰好反应完后,溶液中NO3-的数目为0.3NA | |
| D. | l L pH=l的硫酸溶液中含有的H+数为0.2NA |
3.下列关于有机物的来源、结构与性质说法正确的是( )
| A. | 甲烷是正四面体结构,性质活泼,常温下能与强酸、强碱发生剧烈反应 | |
| B. | 乙烯是通过石油裂解得到的,属于不饱和烃 | |
| C. | 苯与氢气、液溴、浓硝酸的反应类型相同 | |
| D. | 乙酸又名醋酸,其官能团是醚基,可以与乙醇发生反应生成乙酸乙酯 |

 +R3
+R3 $\stackrel{C_{2}H_{5}ONa}{→}$
$\stackrel{C_{2}H_{5}ONa}{→}$ +R2OH
+R2OH .
. .
.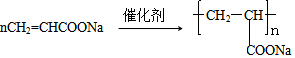 .
. .
. 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系: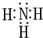 .
.