题目内容
5.将反应2Fe3++Cu=2Cu2++2Fe2+设计成原电池,正极反应为Fe3++e-=Fe2+,10min内该电池向外提供0.1mol电子,则正极材料与负极材料的质量差为3.2g,(假设刚开始时,两电极的质量相等).分析 根据电池反应式知,Cu失电子发生氧化反应,则作负极,不如Cu活泼的金属或导电的非金属作正极,含有铁离子的可溶性铁盐溶液为电解质溶液,根据转移电子与Cu的关系式计算消耗Cu的质量.
解答 解:根据电池反应式知,Cu失电子发生氧化反应,则作负极,不如Cu活泼的金属或导电的非金属作正极,含有铁离子的可溶性铁盐溶液为电解质溶液,如FeCl3溶液,正极的电极反应式为:Fe3++e-═Fe2+;负极反应式为Cu-2e-=Cu2+,负极上铜失电子生成铜离子进入溶液,所以铜质量在不断减少,根据转移电子与Cu的关系式得消耗Cu的质量=$\frac{0.1mol}{2}$×64g/mol=3.2g;
故答案为:Fe3++e-=Fe2+; 3.2.
点评 本题考查原电池设计,侧重考查学生设计及计算能力,会根据得失电子确定原电池正负极、电解质溶液,失电子的金属作负极、得电子的可溶性电解质溶液为该原电池电解质溶液,题目难度不大.

练习册系列答案
相关题目
15.有关乙烯及其相关有机物的结构和性质,下列说法正确的是( )
| A. | 乙烯使酸性高锰酸钾褪色的原理和使溴水褪色的原理相同 | |
| B. | 乙烯不能合成高分子化合物 | |
| C. | 工业制备乙烯通常通过石油的裂解 | |
| D. | 聚乙烯能使溴水褪色 |
16.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. |  3-丁醇 3-丁醇 | C. |  3-甲基-2-戊烯 3-甲基-2-戊烯 | D. |  1,3,4-三甲苯 1,3,4-三甲苯 |
13.参考下列(a)~(c)项回答问题:
(a)皂化值是使1g油脂皂化所需要的KOH的毫克数.
(b)碘值是使100g油脂加成碘的克数.
(c)各种油脂的皂化值、碘值列表如下:
(1)单纯由(C17H33COO)3C3H5(相对分子质量884)形成的油,皂化值是190
(2)在横线上填入适当的词句:
亚麻仁油比花生油所含的碳碳双键多,黄油比牛油的平均相对分子质量小.硬化大豆油的碘值小的原因是硬化大豆油已经过硬化处理,含碳碳双键很少,所以碘值很小.
(3)为使碘值为180的鱼油100g硬化所需要的H2的体积为15.9升(标准状况下)?
(4)结构简式为 的酯,若皂化值为430,求n为4.
的酯,若皂化值为430,求n为4.
(a)皂化值是使1g油脂皂化所需要的KOH的毫克数.
(b)碘值是使100g油脂加成碘的克数.
(c)各种油脂的皂化值、碘值列表如下:
| 花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
| 皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
| 碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(2)在横线上填入适当的词句:
亚麻仁油比花生油所含的碳碳双键多,黄油比牛油的平均相对分子质量小.硬化大豆油的碘值小的原因是硬化大豆油已经过硬化处理,含碳碳双键很少,所以碘值很小.
(3)为使碘值为180的鱼油100g硬化所需要的H2的体积为15.9升(标准状况下)?
(4)结构简式为
 的酯,若皂化值为430,求n为4.
的酯,若皂化值为430,求n为4.
20.白铁皮(镀锌)发生析氢腐蚀时,若转移0.2mol电子,下列说法正确的是( )
| A. | 有6.5 g锌被腐蚀 | B. | 有22.4 L氢气放出 | ||
| C. | 有2.8 g铁被腐蚀 | D. | 有2.24 L氢气放出 |
10.下列有机物在一定条件下自身分子间能发生缩聚反应,而在适宜的条件下分子内又能形成环状结构的是( )
| A. | 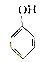 | B. | CH2═CH-Cl | ||
| C. | 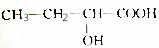 | D. | HO(CH2)4COOH |
17.镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物.工业制备镓的流程如下图所示:
下列判断不合理的是( )

下列判断不合理的是( )
| A. | Al、Ga均处于ⅢA族 | B. | Ga2O3可与盐酸反应生成GaCl3 | ||
| C. | Ga(OH)3可与NaOH溶液生成NaGaO2 | D. | 酸性:Al(OH)3>Ga(OH)3 |