题目内容
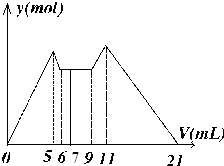 如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )
如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )| A、原混合液中,C(Al3+):C(Mg2+):C(Cl-)=1:1:5 |
| B、A是NaOH,B是盐酸,且C(NaOH):C(HCl)=2:1 |
| C、从7到9,相应离子反应式H++OH-=H2O |
| D、B是盐酸,A是NaOH,且C(B)=C(A) |
考点:离子方程式的有关计算
专题:
分析:A、根据第一次沉淀最大到最小需要的氢氧化钠的量计算铝离子的物质的量,根据需要氢氧化钠总的物质的量计算镁离子的物质的量,根据电荷守恒计算氯离子的物质的量;
B、根据铝元素守恒计算氢氧化钠与盐酸浓度的关系;
C、根据从7到9mL沉淀的物质的量不变,则发生的反应为氢氧化钠与盐酸的反应;
D、根据B的分析判断.
B、根据铝元素守恒计算氢氧化钠与盐酸浓度的关系;
C、根据从7到9mL沉淀的物质的量不变,则发生的反应为氢氧化钠与盐酸的反应;
D、根据B的分析判断.
解答:
解:A、从加入5 mL A生成沉淀最多,再继续加1 mL A沉淀量减少到最小值,相应反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,由此可知,n(Al3+)=n〔Al(OH)3〕=(1×6×10-3) mol;由前5 mL NaOH形成最大沉淀量可知,2n(Mg2+)+3n(Al3+)=(5×10-3×6)mol,所以n(Mg2+)=(1×6×10-3) mol,溶液中阴阳离子所带电荷相等得,n(Cl-)=(5×10-3×6)mol,即溶液中C(Al3+):C(Mg2+):C(Cl-)=1:1:5,故A正确;
B、根据加入前6mL试剂时,先有沉淀生成而后溶解,所以试剂A是NaOH,则B是盐酸;又由图可知,5→6(1 mL)、9→11(2 mL)分别是溶解Al(OH)3和使AlO2-恰好完全生成Al(OH)3沉淀消耗的NaOH和HCl.根据铝元素守恒:
NaOH~Al(OH)3~AlO2-~H+
1 1 1 1
0.001L?c(NaOH) 0.002L?c(HCl)
由此可以推出:c(NaOH):c(HCl)=2:1,故B正确;
C、从7到9mL沉淀的物质的量不变,则发生的反应为氢氧化钠与盐酸的反应,反应的离子方程式为H++OH-=H2O,故C正确;
D、由B分析可知,试剂A是NaOH,B是盐酸,c(NaOH):c(HCl)=2:1,故D错误;
故选D.
B、根据加入前6mL试剂时,先有沉淀生成而后溶解,所以试剂A是NaOH,则B是盐酸;又由图可知,5→6(1 mL)、9→11(2 mL)分别是溶解Al(OH)3和使AlO2-恰好完全生成Al(OH)3沉淀消耗的NaOH和HCl.根据铝元素守恒:
NaOH~Al(OH)3~AlO2-~H+
1 1 1 1
0.001L?c(NaOH) 0.002L?c(HCl)
由此可以推出:c(NaOH):c(HCl)=2:1,故B正确;
C、从7到9mL沉淀的物质的量不变,则发生的反应为氢氧化钠与盐酸的反应,反应的离子方程式为H++OH-=H2O,故C正确;
D、由B分析可知,试剂A是NaOH,B是盐酸,c(NaOH):c(HCl)=2:1,故D错误;
故选D.
点评:本题考查了镁、铝重要化合物的性质,题目难度较大,能正确分析图象中转折线发生的化学反应是解本题的关键,试题有利于培养学生的逻辑思维能力和发散思维能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有一种MCFC型燃料电池,该电池所用燃料为H2和空气,电解质为熔融的K2CO3.电池的总反应为:2H2+O2=2H2O,负极反应为H2+CO32--2e-=H2O+CO2.下列说法中正确的是( )
| A、正极反应为4OH--4e-=2H2O+O2↑ |
| B、电池放电时,电池中CO32-的物质的量将逐渐减少 |
| C、放电时CO32-向负极移动 |
| D、电路中的电子经正极、负极、熔融的K2CO3后再流回正极,形成闭合回路 |
通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如图所示:

下列关于这些晶体结构和性质的叙述不正确的是( )

下列关于这些晶体结构和性质的叙述不正确的是( )
| A、同一主族的不同元素与另一同种元素所形成的化学式相似的物质不一定具有相同的晶体结构 |
| B、氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质 |
| C、二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 |
| D、在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C3->D->B+>A2+ |
| D、原子的最外层电子数目:A>B>D>C |
等质量的下列有机物与足量的金属钠反应,放出氢气最多的是( )
| A、甲醇 | B、乙醇 |
| C、乙二醇 | D、丙三醇 |
将钠块放在坩埚中加热,可观察到的实验现象为( )
①钠块熔化 ②在空气中燃烧产生黄色火焰 ③生成白色固体④生成淡黄色固体 ⑤燃烧时放出大量白烟.
①钠块熔化 ②在空气中燃烧产生黄色火焰 ③生成白色固体④生成淡黄色固体 ⑤燃烧时放出大量白烟.
| A、①②③ | B、①②④ |
| C、②④⑤ | D、①③⑤ |


