题目内容
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C3->D->B+>A2+ |
| D、原子的最外层电子数目:A>B>D>C |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序数:a>b>d>c,结合元素周期律递变规律解答该题.
解答:
解:短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序数:a>b>d>c.
A.A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,原子核外电子层数越多,半径越大,同周期元素原子序数越大,原子半径越小,则有原子半径:B>A>C>D,故A错误;
B.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,所以原子序数:a>b>d>c,故B错误;
C.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数a>b>d>c,所以离子半径C3->D->B+>A2+,故C正确;
D.A、B为同周期金属元素,A离子带的正电荷较多,故最外层电子数A>B,C、D为同周期非金属性元素,C离子所带负电荷较多,故最外层电子数C<D,C、D的族序数大于A、B,故最外层电子数D>C>A>B,故D错误,
故选:C.
A.A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,原子核外电子层数越多,半径越大,同周期元素原子序数越大,原子半径越小,则有原子半径:B>A>C>D,故A错误;
B.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,所以有:a-2=b-1=c+3=d+1,所以原子序数:a>b>d>c,故B错误;
C.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数a>b>d>c,所以离子半径C3->D->B+>A2+,故C正确;
D.A、B为同周期金属元素,A离子带的正电荷较多,故最外层电子数A>B,C、D为同周期非金属性元素,C离子所带负电荷较多,故最外层电子数C<D,C、D的族序数大于A、B,故最外层电子数D>C>A>B,故D错误,
故选:C.
点评:本题考查位置结构性质关系及应用,根据核外电子排布确定元素所在周期表中的位置,理解掌握元素周期律的递变规律,难度不大,注意由于是短周期元素,可以确定具体的元素.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
2006年诺贝尔化学奖授予美国科学家Roger.D.Kormberg,他揭示了真核生物体内的细胞如何利用基因内存储的信息生产蛋白质.下列关于蛋白质的说法中正确的是( )
| A、可以利用多次盐析或多次渗析来分离提纯蛋白质 |
| B、生命活动离不开蛋白质的参与,蛋白质均为天然有机高分子化合物 |
| C、CuSO4溶液或(NH4)2SO4溶液均能使蛋白质变性 |
| D、蛋白质均易溶于水,均既能与盐酸反应,又能与氢氧化钠反应 |
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A、b、a、e、d、c |
| B、e、d、a、b、c |
| C、a、b、d、c、e |
| D、c、d、e、a、b |
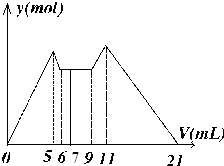 如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )
如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )| A、原混合液中,C(Al3+):C(Mg2+):C(Cl-)=1:1:5 |
| B、A是NaOH,B是盐酸,且C(NaOH):C(HCl)=2:1 |
| C、从7到9,相应离子反应式H++OH-=H2O |
| D、B是盐酸,A是NaOH,且C(B)=C(A) |
下列推断合理的是( )
| A、氯化铝和氯化铁在水中都能形成胶体,都可用作净水剂 |
| B、金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| C、浓HNO3有强氧化性,常温下能与Fe发生剧烈反应 |
| D、将SO2通入溴水,溴水褪色后加热能恢复原色 |
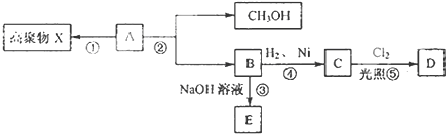
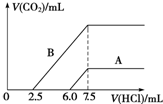 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.
含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.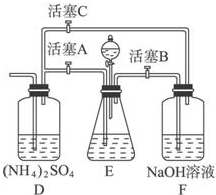 摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂.某研究性学习小组设计了下面的实验装置来制备摩尔盐.
摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂.某研究性学习小组设计了下面的实验装置来制备摩尔盐.