题目内容
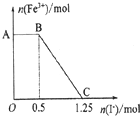 已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、根据OC段数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D、根据OC段的数据可知开始加入的硫酸亚铁的物质的量为l mol |
考点:化学方程式的有关计算
专题:图示题,计算题
分析:氧化性强弱顺序为KMnO4>Fe3+,由图象可知,在反应后的溶液中滴加碘化钾溶液,开始时Fe3+浓度不变,则说明Fe3+没有参加反应,则AB应为高锰酸钾和碘化钾的反应,BC段为铁离子和碘化钾的反应,结合得失电子守恒解答该题.
解答:
解:A.开始时Fe3+浓度不变,则说明Fe3+没有参加反应,则AB应为高锰酸钾和碘化钾的反应,故A正确;
B.BC段Fe3+浓度逐渐减小,为铁离子和碘化钾的反应,反应的离子方程式为2Fe3++2I-=2Fe2++I2,故B正确;
C.由氧化剂和还原剂得失电子数目相等可知反应的关系式为2KMnO4~10Fe3+~10I-,共消耗的n(I-)=1.25mol,则开始加入的高锰酸钾的物质的量为
mol=0.25mol,故C正确;
D.由方程式2Fe3++2I-→2Fe2++I2可知,BC段消耗KI0.75mol,则n(Fe3+)=n(Fe2+)=0.75mol,故D错误.
故选D.
B.BC段Fe3+浓度逐渐减小,为铁离子和碘化钾的反应,反应的离子方程式为2Fe3++2I-=2Fe2++I2,故B正确;
C.由氧化剂和还原剂得失电子数目相等可知反应的关系式为2KMnO4~10Fe3+~10I-,共消耗的n(I-)=1.25mol,则开始加入的高锰酸钾的物质的量为
| 1.25 |
| 5 |
D.由方程式2Fe3++2I-→2Fe2++I2可知,BC段消耗KI0.75mol,则n(Fe3+)=n(Fe2+)=0.75mol,故D错误.
故选D.
点评:本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握反应的相关方程式的书写,根据方程式、关系式计算该题,难度中等.

练习册系列答案
相关题目
柠檬烯醇是一种实用香精,其结构简式如图所示.下列有关柠檬烯醇的说法正确的是( )
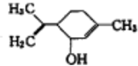

| A、能与氢氧化钠溶液发生中和反应 |
| B、能发生加成反应和取代反应 |
| C、不能使酸性高锰酸钾溶液褪色 |
D、与对丙基苯甲醇(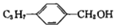 )互为同分异构体 )互为同分异构体 |
下面的排序不正确的是( )
| A、晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B、熔点由高到低:Na>Mg>Al |
| C、硬度由大到小:金刚石>碳化硅>晶体硅 |
| D、电负性由大到小:F>O>S |
为了检验某固体物质中是否含有NH4+,你认为下列试纸和试剂一定用不到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸.
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸.
| A、①⑤ | B、④⑤ |
| C、①③⑤ | D、①④⑤ |
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子.则该硫酸盐的物质的量浓度为( )
| A、2 mol?L-1 |
| B、2.5 mol?L-1 |
| C、5 mol?L-1 |
| D、7.5 mol?L-1 |
如今人们把食品分为绿色食品、蓝色食品、白色食品等类型.绿色植物通过光合作用转化的食品叫绿色食品;而直接从海洋获取的食品叫蓝色食品;可通过微生物发酵制得的食品叫白色食品.下面属于白色食品的( )
| A、乙醇 | B、面粉 | C、海带 | D、食盐 |
粗盐提纯实验的部分操作如图所示,其中错误的是( )
A、 取一定量的粗盐 |
B、 溶解 |
C、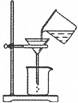 过滤 |
D、 蒸发 |
下列溶液一定是碱性的是( )
| A、pH>7的某电解质的溶液 |
| B、c(OH-)>1×10-7mol/L |
| C、溶液中含有OH- |
| D、溶液中c(OH-)>c(H+) |