题目内容
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子.则该硫酸盐的物质的量浓度为( )
| A、2 mol?L-1 |
| B、2.5 mol?L-1 |
| C、5 mol?L-1 |
| D、7.5 mol?L-1 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:1.5NA个硫酸根离子的物质的量为1.5mol,NA个金属阳离子的物质的量为1mol,根据电荷守恒可知,金属阳离子为+3价,所以该硫酸盐可以表示为M2(SO4)3,根据硫酸根守恒可知,硫酸盐为0.5mol,再利用c=
计算.
| n |
| V |
解答:
解:1.5NA个硫酸根离子的物质的量为1.5mol,NA个金属阳离子的物质的量为1mol,令金属离子的化合价为x,根据电荷守恒可知,x=1.5×2=3,故金属阳离子为+3价,所以该硫酸盐可以表示为M2(SO4)3,根据硫酸根守恒可知,硫酸盐为0.5mol,所以该硫酸盐的物质的量浓度为
=2.5mol/L.
故选:B.
| 0.5mol |
| 0.2L |
故选:B.
点评:考查物质的量浓度计算,难度中等,判断金属离子的化合价是解题关键,注意守恒思想的运用.

练习册系列答案
相关题目
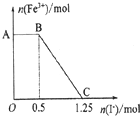 已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、根据OC段数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D、根据OC段的数据可知开始加入的硫酸亚铁的物质的量为l mol |
有机物分子中原子或原子团间的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| B、乙醇与金属钠反应没有水与金属钠反应剧烈 |
| C、甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 |
| D、苯酚能与NaOH溶液反应,而乙醇不能与NaOH溶液反应 |
检验SO2气体中是否混有CO2气体,可采用的方法是( )
| A、通过品红溶液 |
| B、通过盐酸,再通过BaCl2溶液 |
| C、先通过NaOH溶液,再通过澄清石灰水 |
| D、先通过酸性KMnO4溶液,再通过澄清石灰水 |
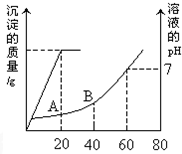
将某些化学知识用数轴表示直观形象、简明易记.下列用数轴表示不正确的是( )
A、碳在氧气中燃烧,n(C)/n(O2)与生成物的关系: |
B、分散系的分类与分散质粒直径大小关系: |
C、AlCl3和NaOH反应后铝元素的存在形式与反应物中n(OH-)/n(Al3+) |
D、Na与O2反应的产物与反应物n(Na)/n(O2)的关系: |
 (1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=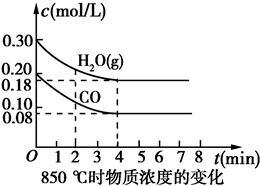 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示: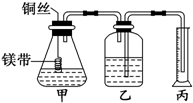 某研究性学习小组为证明在同温同压下,相同浓度、相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度、相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤如下: