题目内容
下列溶液一定是碱性的是( )
| A、pH>7的某电解质的溶液 |
| B、c(OH-)>1×10-7mol/L |
| C、溶液中含有OH- |
| D、溶液中c(OH-)>c(H+) |
考点:溶液pH的定义
专题:电离平衡与溶液的pH专题
分析:溶液的酸碱性是根据溶液中氢离子浓度和氢氧根离子浓度的相对大小判断的,当溶液中c(OH-)<c(H+)时,溶液呈酸性;当c(OH-)=c(H+)时,溶液呈中性;当c(OH-)>c(H+)时,溶液呈碱性,注意不能根据溶液的pH值大小判断.
解答:
解:A、温度影响水的电离,温度降低,水的电离程度减小,溶液中氢离子浓度减小,所以pH>7的溶液中不能判断c(OH-)与c(H+)的关系,故A错误;
B、温度影响水的电离,温度升高,水的电离程度增大,中性溶液中氢氧根离子离子浓度增大,所以c(OH-)>1×10-7mol/L溶液中不能判断c(OH-)与c(H+)的关系,故B错误;
C、任何溶液中都存在氢离子、氢氧根离子,所以含有OH-离子的溶液不一定显示碱性,故C错误;
D、溶液中c(OH-)>c(H+)的溶液,溶液一定碱性,故D正确;
故选D.
B、温度影响水的电离,温度升高,水的电离程度增大,中性溶液中氢氧根离子离子浓度增大,所以c(OH-)>1×10-7mol/L溶液中不能判断c(OH-)与c(H+)的关系,故B错误;
C、任何溶液中都存在氢离子、氢氧根离子,所以含有OH-离子的溶液不一定显示碱性,故C错误;
D、溶液中c(OH-)>c(H+)的溶液,溶液一定碱性,故D正确;
故选D.
点评:本题考查了溶液PH的计算和溶液酸碱性的判断依据,水的离子积的计算应用,注意不能根据溶液的PH值大小判断溶液酸碱性,试题贴近高考,针对性强,有利于激发学生的学习兴趣和学习积极性.

练习册系列答案
相关题目
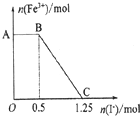 已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、根据OC段数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D、根据OC段的数据可知开始加入的硫酸亚铁的物质的量为l mol |
某工厂用硫酸处理氨气尾气,得到铵盐(不同批次得到a、b、c三种不同的铵盐).称取不同质量的铵盐,加入到固定量的NaOH溶液中并加热,收集氨气,得到如下生成氨气的量与加入铵盐的量关系图:下列判断不正确的是( )
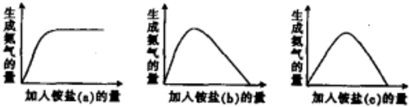

| A、a对应的铵盐是(NH4)2SO4 |
| B、b对应的铵盐是(NH4)2SO4和NH4HSO4 |
| C、c对应的铵盐是NH4HSO4 |
| D、当b和c铵盐的质量相同时,可得到相同量的氨气 |
药物是人们生活的必备品之一,下列药物的主要成分都能发生以下四种反应的是( )
①取代反应②加成反应③水解反应④中和反应

①取代反应②加成反应③水解反应④中和反应

| A、维生素 | B、阿司匹林 |
| C、芬必得 | D、扑热息痛 |
在某无色透明的酸性溶液中,能共存的离子组是( )
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、AlO2-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
将金属钠分别投入下列物质的溶液中,有气体放出,且溶液质量减轻的是( )
| A、稀盐酸 |
| B、K2SO4 |
| C、CuCl2 |
| D、NaOH溶液 |
下列说法正确的是( )
| A、含硅材料广泛用于太阳能电板、半导体材料、光纤通讯以及建筑材料等 |
| B、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| C、工艺师利用稀盐酸刻蚀石英制作艺术品 |
| D、粗硅制备单晶硅不涉及氧化还原反应 |
下列有关物质的性质比较,不正确的是( )
| A、熔点:Li>Cs |
| B、还原性:F->I- |
| C、热稳定性:H2O>H2S |
| D、酸性:H3PO4>H3AsO4 |