题目内容
为了检验某固体物质中是否含有NH4+,你认为下列试纸和试剂一定用不到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸.
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸.
| A、①⑤ | B、④⑤ |
| C、①③⑤ | D、①④⑤ |
考点:铵离子检验
专题:氮族元素
分析:依据铵盐能够与碱反应生成氨气的性质,通过检验铵盐与碱的反应产物有氨气的存在即可证明物质是否含氨根离子,而氨气能使湿润的红色石蕊试纸变蓝色,据此分析解答.
解答:
解:铵根离子和氢氧化钠溶液反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色,则需要红色石蕊试纸,且需要蒸馏水润湿试纸,则不需要的物质是蓝色石蕊试纸及稀硫酸,
故选B.
故选B.
点评:本题考查了氨根离子的检验,明确铵盐、氨气的性质是解题关键,注意指示剂的选择.

练习册系列答案
相关题目
下列反应中生成物总能量高于反应物总能量的是( )
| A、炭和水蒸气反应 |
| B、乙醇燃烧 |
| C、铝粉与氧化铁粉末反应 |
| D、氧化钙溶于水 |
设计如图所示的装置研究电化学原理,下列叙述错误的是( )
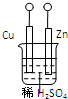

| A、a、b不连接时,只锌片上有气泡逸出,锌片逐渐溶解 |
| B、a和b用导线连接时,H+从铜片上获得锌失去的电子 |
| C、a和b是否用导线连接,装置中所涉及的化学反应都相同 |
| D、a和b是否用导线连接,装置中都是化学能转变为电能过程 |
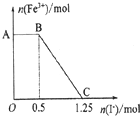 已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、根据OC段数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D、根据OC段的数据可知开始加入的硫酸亚铁的物质的量为l mol |
要使含有Ag+、Cu2+、Mg2+、Ba2+等离子的溶液中的离子逐一形成沉淀析出,下列所选择试剂及加入试剂的顺序正确的是( )
| A、H2SO4→HCl→K2S→NaOH→CO2 |
| B、Na2SO4→NaCl→Na2S→NH3?H2O |
| C、NaCl→Na2SO4→H2S→NaOH |
| D、Na2S→Na2SO4→NaCl→NaOH |
在某无色透明的酸性溶液中,能共存的离子组是( )
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、AlO2-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
 实验室欲配制0.05mol?L-1的NaOH溶液500mL,有以下仪器:
实验室欲配制0.05mol?L-1的NaOH溶液500mL,有以下仪器: