题目内容
4.有关如图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是( )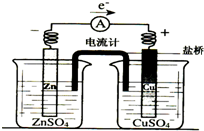
| A. | 铜片上有气泡逸出 | |
| B. | 取出盐桥后,电流计依然发生偏转 | |
| C. | 反应中,盐桥中的K+会移向CuSO4溶液 | |
| D. | 铜片上发生氧化反应 |
分析 图为原电池装置,Zn为负极,发生氧化反应Zn-2e-═Zn2+,Cu为正极,发生还原反应Cu2++2e-═Cu,原电池工作时,阳离子向正极移动,阴离子向负极移动,以此解答该题.
解答 解:A.Cu为正极,发生还原反应Cu2++2e-═Cu,析出Cu,无气泡产生,故A错误;
B.取出盐桥后,不是闭合回路,没有电流产生,电流计不发生偏转,故B错误;
C.原电池工作时,阳离子向正极移动,阴离子向负极移动,盐桥中的K+会移向CuSO4溶液,故C正确;
D.Cu为正极,发生还原反应Cu2++2e-═Cu,故D错误,
故选:C.
点评 本题考查原电池的工作原理,题目难度不大,注意电极的判断和电极方程式的书写,把握原电池的工作原理,学习中注意相关知识的把握.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
12.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol/L Na2CO3溶液:c(OH-)+c(H+)═c(HCO3-)+2c(H2CO3) | |
| B. | 0.1mol/L NH4Cl溶液:c(NH4+)+c(Cl-)═0.2mol/L | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=4的混合溶液:c(Na+)═c(NO3-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
15.下列指定微粒的数目不相等的是( )
| A. | 等物质的量的水与重水含有的电子数 | |
| B. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| C. | 同温、同压、同体积的CO和NO含有的原子数 | |
| D. | 常温下等物质的量的铝分别与足量氯气、浓硝酸反应时转移的电子数 |
12.下列物质中既能与酸性KMnO4溶液反应,又能与溴水反应的一组物质是( )
①苯 ②苯乙烯 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸
⑧聚丁二烯 ⑨聚乙烯 ⑩聚乙炔.
①苯 ②苯乙烯 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸
⑧聚丁二烯 ⑨聚乙烯 ⑩聚乙炔.
| A. | ②⑤⑧⑨⑩ | B. | ②④⑥⑦ | C. | ②⑤⑦⑧⑩ | D. | ①②③④⑤⑥⑦⑧ |
19.室温时,下列混合溶液的pH一定小于7的是( )
| A. | pH=3的盐酸和pH=11的氨水等体积混合 | |
| B. | 0.1mol/L的盐酸和0.1mol/L的氢氧化钡溶液等体积混合 | |
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 | |
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
9.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:Cl>S | ||
| C. | 热稳定性Na2CO3>NaHCO3 | D. | 碱性:NaOH>Mg(OH)2 |
16.下列各组的电极材料和电解液,不能组成原电池的是( )
| A. | 铜片、铜片、稀硫酸 | B. | 铜片、石墨棒、硝酸银溶液 | ||
| C. | 锌片、铜片、稀硫酸 | D. | 铜片、银片、FeCl3溶液 |
13.下列有关物质用途的说法中,不正确的是( )
| A. | Fe2O3常用作红色油漆和涂料 | B. | 碳酸氢钠可用于治疗胃酸过多 | ||
| C. | 二氧化硅可用于制造集成电路 | D. | Cl2可用于制漂白粉 |
14.已知在1×105Pa、298K的条件下,2mol H2燃烧生成水蒸气时放出484kJ热量,下列热化学方程式正确的是( )
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=242 kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=242 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1 |