题目内容
14.已知在1×105Pa、298K的条件下,2mol H2燃烧生成水蒸气时放出484kJ热量,下列热化学方程式正确的是( )| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=242 kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=242 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1 |
分析 A、水分解反应是吸热反应,2mol氢气燃烧生成水蒸气放出484kJ热量,则1mol氢气燃烧生成水蒸气放出242kJ热量,其逆过程就要吸收这些热量;
B、是生成水蒸气,而不是液态水;
C、2mol氢气燃烧生成水蒸气放出484kJ热量,则1mol氢气燃烧生成水蒸气放出242kJ热量,所以H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol2mol氢气;
D、燃烧生成水蒸气放出484kJ热量,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol.
解答 解:A、2mol氢气燃烧生成水蒸气放出484kJ热量,则1mol氢气燃烧生成水蒸气放出242kJ热量,其逆过程就要吸收这些热量,有:H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H=+242kJ•mol-1,+号不能省略,故A错误;
B、是生成水蒸气,而不是液态水,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,故B错误;
C、放热而不是吸热,所以1mol氢气燃烧生成水蒸气放出242kJ热量,所以H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol,故C错误;
D、2mol氢气燃烧生成水蒸气放出484kJ热量,所以热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,故D正确;
故选D.
点评 本题主要考查学生热化学方程式的书写原则,主要是反应焓变的计算,反应改变方向,焓变改变符号,该题型是现在高考的热点,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.有关如图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是( )
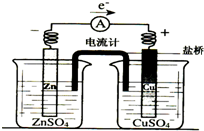

| A. | 铜片上有气泡逸出 | |
| B. | 取出盐桥后,电流计依然发生偏转 | |
| C. | 反应中,盐桥中的K+会移向CuSO4溶液 | |
| D. | 铜片上发生氧化反应 |
5.如果慢慢把下列溶液加热蒸干并灼烧,可以得到该溶液溶质固体的是( )
| A. | 高锰酸钾 | B. | 亚硫酸钠 | C. | 氯化铁 | D. | 碳酸钾 |
9.化学在生活中无处不在,下列说法错误的是( )
| A. | 炒菜时加入一些料酒和食醋,这样可使菜变得味香可口,这是因为有酯类物质生成 | |
| B. | 禁止使用工业酒精配制料酒,这是因为工业酒精中常含有少量会使人中毒的甲醇 | |
| C. | 苯酚不小心蘸到皮肤上,应用NaHCO3溶液擦洗 | |
| D. | 夏季蚊虫较多,一旦被叮咬,就会感到皮肤瘙痒,这是由于蚊虫的分泌液中含有甲酸 |
19.实验室欲制氢气,所用稀盐酸和稀硫酸的浓度相同,反应速率最快的是( )
| A. | 纯锌与稀硫酸反应 | B. | 纯锌和浓硫酸反应 | ||
| C. | 纯锌与稀盐酸反应 | D. | 粗锌(含铅、铜杂质)与稀硫酸反应 |
6.有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚乙烯;⑧环己烯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A. | ①②③⑤ | B. | ④⑥⑦⑧ | C. | ①④⑥⑦ | D. | ②③⑤⑧ |
3.下列各化合物的命名中正确的是( )
| A. | CH2═CH-CH═CH2 1,3-二丁烯 | B. | CH3-CH2-CH═CH2 3-丁烯 | ||
| C. | 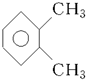 对二甲苯 对二甲苯 | D. | 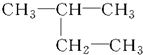 3-甲基丁烷 3-甲基丁烷 |
4.对于A2+3B2=2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | v(A2)=0.4 mol•L-1•s-1 | B. | v(B2)=0.8 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=0.6 mol•L-1•min-1 |
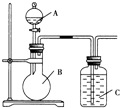 某甲同学设计如图装置,比较非金属元素的非金属性强弱.请按要求回答下列问题:
某甲同学设计如图装置,比较非金属元素的非金属性强弱.请按要求回答下列问题: