题目内容
3. 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式3d84s2,它位于周期表d区.
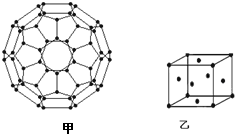
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为sp2;1mol C60分子中σ键的数目为90NA个.
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等.
①第一电离能:As>Ga(填“>”、“<”或“=”).
②SeO2分子的空间构型为V形.
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4NH3 Cu NF3+3NH4F,该反应中
NH3的沸点<(填“>”、“<”或“=”)HF的沸点,NH4F固体属于离子晶体.往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子.图乙为一个金属铜的晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为$\frac{256×10{\;}^{30}}{ρa{\;}^{3}}$ mol-1(用含a、ρ的代数式表示).
分析 (1)28号元素镍,核外有28个电子,根据构造原理写出其基态镍原子的核外电子排布式,根据价电子排布式确定分区;
(2)根据价层电子对互斥理论确定杂化方式,利用均摊法计算每个碳原子含有几个σ键,从而计算1mol C60分子中σ键的数目;
(3)①同一周期元素的第一电离能随着原子序数的增大而增大,但第VA族元素第一电离能大于第VIA元素;
②根据价层电子对互斥理论确定其空间构型;
(4)F的电负性大于N,形成的氢键强度F-H>N-H,因此HF的沸点大于NH3的沸点;NH4F是由NH4+和F-构成的离子化合物,属于离子晶体;N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子;根据均摊法计算晶胞中Cu原子数目,结合相对分子质量及阿伏伽德罗常数表示出晶胞质量,根据晶胞棱长计算晶胞体积,再根据密度计算晶胞质量,据此列方程计算.
解答 解:(1)28号元素镍,核外有28个电子,根据构造原理知其基态镍原子的核外电子排布式的简化形式为[Ar]3d84s2,因此基态镍原子的外围电子排布式为3d84s2,位于周期表d区,
故答案为:3d84s2;d;
(2)每个碳原子含有的σ键个数且不含孤电子对,所以采用sp2 杂化,每个碳原子含有的σ键个数为$\frac{3}{2}$,所以1mol C60分子中σ键的数目=$\frac{3}{2}$×60NA=90NA,
故答案为:sp2;90NA;
(3)①As和Se属于同一周期,且As属于第VA族,Se属于第VIA族,所以第一电离能As>Se,
故答案为:>;
②二氧化硒分子中价层电子对=2+$\frac{1}{2}$(6-2×2)=3,且含有一个孤电子对,所以属于V形,
故答案为:V形;
(4)F的电负性大于N,形成的氢键强度F-H>N-H,因此HF的沸点大于NH3的沸点;NH4F是由NH4+和F-构成的离子化合物,属于离子晶体;
N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子;
晶胞中含有铜原子数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则晶胞质量为$\frac{4×64}{N{\;}_{A}}$g,该晶胞体积为a3 pm3,则$\frac{4×64}{N{\;}_{A}}$g=a3 pm3×ρ g/cm3,故NA=$\frac{256×10{\;}^{30}}{ρa{\;}^{3}}$,
故答案为:<;离子;F的电负性大于N,NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键;=$\frac{256×10{\;}^{30}}{ρa{\;}^{3}}$;
点评 本题是对物质结构的考查,涉及核外电子排布式、电离能、分子结构、杂化轨道、配合物、晶胞计算等,难度中等,注意利用均摊法进行晶胞有关计算,理解同周期第一电离能突跃原因.

| A. | SO2具有还原性,故可作漂白剂 | |
| B. | Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg | |
| C. | HClO见光会分解,故氯水保存在棕色试剂瓶中 | |
| D. | Fe在Cl2中燃烧生成FeCl3,故在与其它非金属反应的产物中的Fe也显+3价 |
| A. | 向AlCl3溶液中逐滴加入氨水,产生白色沉淀后消失 | |
| B. | 向Na2SiO3溶液中逐滴加入稀盐酸,产生白色胶状沉淀 | |
| C. | 钠与氧气在加热条件下反应,生成白色固体 | |
| D. | 将砂纸打磨过的铝箔加热至熔化,熔化的铝以小液滴的形式滴落下来 |
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
①向废液中加入甲溶液;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入乙溶液(过量),然后再放入蒸馏器中进行蒸馏,收集馏出物.
可选用试剂:A.烧碱溶液 B.浓硫酸 C.饱和食盐水 D.浓盐酸
请回答下列问题:
(l)乙醇的沸点比丙酮沸点高的主要原因是乙醇分子之间易形成氢键.
(2)加入甲溶液是A,(填A B C D序号),涉及到的反应方程式:CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH、CH3COOH+NaOH→CH3COONa+H2O.
(3)在70℃~85℃时馏出物的主要成分为乙醇.
(4)在步骤④中加入过量的乙溶液是B.(填A B C D序号),
(5)最后蒸馏的温度控制在117.9℃左右.
(6)在蒸馏操作中,仪器选择及安装都正确的是:(填标号)
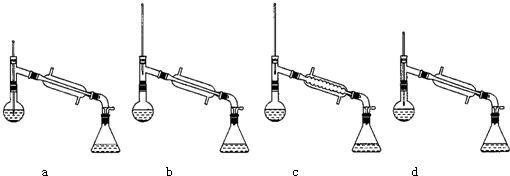
如果蒸馏前忘记加沸石,液体温度已接近沸点时,应该如何处理?b;移开热源,待温度降低,再投入沸石,重新加热.
| A. | 锌粒与稀硫酸反应时,加入少量醋酸钠,则反应速率降低 | |
| B. | 醋酸比硫酸对衣服的腐蚀性差 | |
| C. | 0.1 mol•L-1醋酸钠溶液的pH约为9 | |
| D. | 用NaOH溶液中和等体积,相同pH的盐酸和醋酸,盐酸消耗NaOH溶液的体积小 |
| A. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用,所以用铝制容器存放盐酸 | |
| B. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| D. | 铝既可以与强酸反应又可以与强碱反应 |
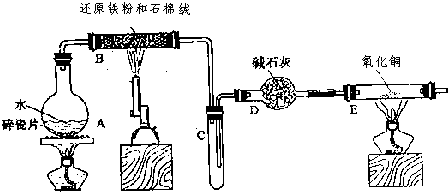
 如图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成.请你用中学化学常见试剂设计一个实验.通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论.试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处.
如图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成.请你用中学化学常见试剂设计一个实验.通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论.试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处.