题目内容
8.根据下列化学方程式:①2FeCl3+2KI=2FeCl2+I2+2KCl②6FeCl3+3Br2=2FeBr3+4FeC13.
分析有关离子的还原性由弱到强的顺序是( )
| A. | Br-<Fe2+<I- | B. | I-<Fe2+<Br- | C. | Br-<I-<Fe2+ | D. | Fe2+<Br-<I- |
分析 依据氧化还原反应的强弱规律,根据元素的化合价升高来判断还原剂,利用氧化还原反应中还原剂的还原性大于还原产物的还原性来解答.
解答 解:①2FeCl3+2KI=2FeCl2+I2+2KCl,I元素的化合价升高,Fe化合价降低,由还原剂的还原性大于还原产物的还原性,则还原性I->Fe2+,
②6FeCl2+3Br2=2FeBr3+4FeC13中,Fe元素的化合价升高,Br化合价降低,由还原剂的还原性大于还原产物的还原性,则还原性Fe2+>Br-,
所以离子的还原性由强到弱的顺序为I->Fe2+>Br-,
故选A.
点评 本题考查了根据方程式来比较氧化性和还原性,解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物,题目难度不大.

练习册系列答案
相关题目
18.NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol•L-1的NaOH溶液中的Na+数目为NA | |
| B. | 标准状况下NA个SO3分子体积约为22.4L | |
| C. | 同温同压下体积相同的任何气体,它们所含的原子数目一定相等 | |
| D. | 含有1 molFe(OH)3的胶体中所含的Fe(OH)3胶粒数小于NA |
19.下列离子方程式正确的是( )
| A. | 向NaClO溶液中通入少量SO2 2ClO-+SO2+H2O=2HClO+SO${\;}_{3}^{2-}$ | |
| B. | 向Fe2(SO4)3溶液中通入足量的H2S Fe3++H2S=Fe2++S↓+2H+ | |
| C. | 向FeBr2中通入等量Cl2 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D. | Fe(OH)3和HI的反应 Fe(OH)3+3H+=Fe3++3H2O |
3.相同温度下,相同物质的量浓度的下列溶液:①NaClO、②NH4NO3、③K2SO4、④NaHSO4、⑤NH3•H2O,按pH由大到小顺序排列正确的是( )
| A. | ⑤①③②④ | B. | ④②③①⑤ | C. | ①⑤③②④ | D. | ①⑤③④② |
13.某烃的相对分子质量为70,该烃能使溴的CCl4溶液褪色则该烃的结构最多有(不考虑立体异构)( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 4种 |
6.一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
下列说法正确的是( )
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 达到平衡时,容器I中的CH3OH体积分数与容器Ⅱ相等 | |
| B. | 容器I中反应的平衡常数K=0.08 | |
| C. | 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向逆反应方向进行 | |
| D. | 容器I中反应达到平衡所需时间比容器Ⅲ中的长 |
3.进入冬季,大雪也会引发巨大灾难.下列说法不正确的是( )
| A. | 雪是由水蒸气凝华而成的,该过程有能量放出 | |
| B. | 雪融化为水后能量增加 | |
| C. | 雪融化为水时要吸收能量,导致环境温度升高 | |
| D. | 在雪上撒大量的盐(如NaCl、MgCl2等)可以融雪 |
4.下列说法或表述中正确的是( )
| A. | 某有机化合物完全燃烧生成等物质的量的CO2和H2O,则该有机物的分子式一定CnH2n | |
| B. | 烷烃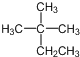 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 | |
| C. | 如图所示的有机物分子式为C14H12O2,能发生银镜反应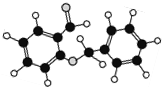 | |
| D. | 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |