题目内容
18.NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 0.1 mol•L-1的NaOH溶液中的Na+数目为NA | |
| B. | 标准状况下NA个SO3分子体积约为22.4L | |
| C. | 同温同压下体积相同的任何气体,它们所含的原子数目一定相等 | |
| D. | 含有1 molFe(OH)3的胶体中所含的Fe(OH)3胶粒数小于NA |
分析 A、溶液体积不明确;
B、标况下三氧化硫为固体;
C、气体分为单原子分子、双原子分子和多原子分子;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答 解:A、溶液体积不明确,故溶液中的钠离子的个数无法计算,故A错误;
B、标况下三氧化硫为固体,故NA个三氧化硫分子的物质的量为1mol,但体积小于22.4L,故B错误;
C、气体分为单原子分子、双原子分子和多原子分子,故同温同压下,相同体积的任何气体的物质的量相同,但含有的原子个数不一定相同,故C错误;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故胶粒的个数小于NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
8.对于某些离子的检验及结论一定正确的是 ( )
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| B. | 加入氢氧化钠溶液,先产生白色沉淀,后迅速变为灰绿色,最后变为红褐色,一定有Fe2+ | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
6.分类是化学研究常用的方法.下列对物质分类正确的是( )
| A. | 氢氧化钾和氧化汞都属于氧化物 | B. | 氧气和臭氧都属于单质 | ||
| C. | 碳酸钙和甲烷都属于有机物 | D. | 火碱和纯碱都属于碱 |
13.有机物分子里的某些原子(或原子团)被其他原子(或原子团)所替代的反应叫取代反应.下列化学反应中不属于取代反应的是( )
| A. | CH2Cl2+Br2$\stackrel{光照}{→}$CHBrCl2+HBr | |
| B. | CH3OH+HCl→CH3Cl+H2O | |
| C. | CH3-CH2-Br+H2O$\stackrel{NaOH}{→}$CH3-CH2-OH+HBr | |
| D. | 2Na+2H2O═2NaOH+H2↑ |
10.下列溶液中Na+与50mL 3mol•L-1 NaCl溶液中Na+物质的量浓度相等的是( )
| A. | 150 mL 1 mol•L-1Na3PO4溶液 | B. | 75 mL 2 mol•L-1NaNO3溶液 | ||
| C. | 75 mL 3 mol•L-1Na2SO4溶液 | D. | 150 mL 2mol•L-1 CH3COONa溶液 |
7.根据碘与氢气反应的热化学方程式:
①I2(g)+H2(g)?2HI(g)△H=-9.48kJ•mol-1
②I2(s)+H2(g)?2HI(g)△H=+26.48kJ•mol-1
下列判断中正确的是( )
①I2(g)+H2(g)?2HI(g)△H=-9.48kJ•mol-1
②I2(s)+H2(g)?2HI(g)△H=+26.48kJ•mol-1
下列判断中正确的是( )
| A. | 254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ | |
| B. | 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ | |
| C. | 反应①的产物比反应②的产物稳定 | |
| D. | 物质的量相同时,反应②的反应物总能量比反应①的反应物总能量低 |
8.根据下列化学方程式:①2FeCl3+2KI=2FeCl2+I2+2KCl
②6FeCl3+3Br2=2FeBr3+4FeC13.
分析有关离子的还原性由弱到强的顺序是( )
②6FeCl3+3Br2=2FeBr3+4FeC13.
分析有关离子的还原性由弱到强的顺序是( )
| A. | Br-<Fe2+<I- | B. | I-<Fe2+<Br- | C. | Br-<I-<Fe2+ | D. | Fe2+<Br-<I- |

 ),M的一种合成路线如图(部分反应试剂和条件省略).
),M的一种合成路线如图(部分反应试剂和条件省略).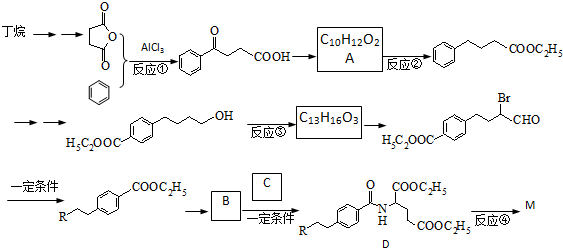
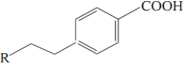 ,C
,C ;
;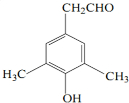 或
或